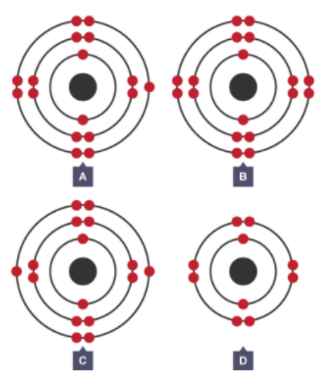
Cho hình vẽ biểu diễn kích thước của các nguyên tử Na, K, F, Cl dưới đây:

Biết số thứ tự của Na, K, F, Cl trong bảng tuần hoàn hoá học lần lượt là 11, 19, 9, 17. Phát biểu nào sau đây đúng?
Trả lời bởi giáo viên
Cấu hình nguyên tử của
- Na (Z=11): 1s22s22p63s1 => Nhóm IA, chu kì 3
- K (Z=19): 1s22s22p63s23p64s1 => Nhóm IA, chu kì 4
- F (Z=9): 1s22s22p5 => Nhóm VIIA, chu kì 2
- Cl (Z=17): 1s22s22p63s23p5 => Nhóm VIIA, chu kì 3
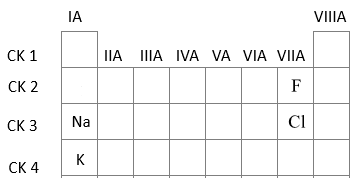
- Trong cùng 1 nhóm A theo chiều tăng dần điện tích hạt nhân, bán kính nguyên tử tăng dần
=> \({r_{Na}} < {r_K}\) và \({r_F} < {r_{Cl}}\) (1)
- Trong cùng 1 chu kì theo chiều tăng dần điện tích hạt nhân, bán kính nguyên tử giảm dần
=> \({r_{Cl}} < {r_{Na}}\)(2)
Từ (1) và (2) => \({r_F} < {r_{Cl}} < {r_{Na}} < {r_K}\)
=> X là F, Y là Cl, Z là Na và T là K
Hướng dẫn giải:
Viết cấu hình electron nguyên tử các nguyên tố => Xác định vị trí nguyên tố trong bảng tuần hoàn
Áp dụng quy luật biến đổi tuần hoàn về bán kính nguyên tử của các nguyên tố