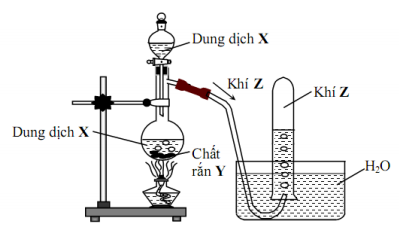
Đốt cháy 13,7 ml hỗn hợp A gồm metan, propan và cacbon (II) oxit, ta thu được 25,7 ml khí CO2 ở cùng điều kiện nhiệt độ và áp suất. Thành phần % thể tích propan trong hỗn hợp A và khối lượng phân tử trung bình của hỗn hợp A so với nitơ là :
Trả lời bởi giáo viên
Đặt số mol của metan, propan và cacbon (II) oxit lần lượt là x, y, z
Sơ đồ phản ứng :
CH4 CO2 (1) ; C3H8 3CO2 (2) ; CO CO2 (3)
x x y 3y z z
Từ (1), (2), (3) và giả thiết ta có hệ :
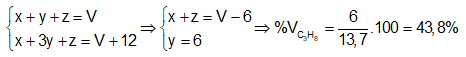
Khối lượng mol trung bình của hỗn hợp A là :
\({\overline M _A} = \dfrac{{16x + 44y + 28z}}{{x + y + z}} > \dfrac{{16(x + z) + 44y}}{{x + y + z}} = \dfrac{{16.7,7 + 44.6}}{{13,7}} = 28,3\,\,gam/mol\)
Mặt khác
\({M_{{N_2}}} = 28\,\,gam/mol\) nên suy ra khối lượng phân tử trung bình của A lớn hơn so với N2 hay \(\dfrac{{\overline M {}_A}}{{{M_{{N_2}}}}} > 1.\)
Hướng dẫn giải:
CH4 CO2 (1) ; C3H8 3CO2 (2) ; CO CO2 (3)
x x y 3y z z
Từ (1), (2), (3) và giả thiết ta có hệ :
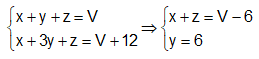
+) \({\overline M _A} = \dfrac{{16x + 44y + 28z}}{{x + y + z}} => \dfrac{{16(x + z) + 44y}}{{x + y + z}}\)
Mặt khác
\({M_{{N_2}}} = 28\,\,gam/mol\) nên suy ra khối lượng phân tử trung bình của A lớn hơn so với N2 hay \(\dfrac{{\overline M {}_A}}{{{M_{{N_2}}}}} > 1.\)