Một nguyên tử có cấu hình electron: 1s2 2s2 2p6 3s2 3p4 a) xác định vị trí của nguyên tố đó trong bảng tuần hoàn ( nêu rõ cách xác định ) đó là ng tố nào b) viết sơ đồ electron tạo phân tử hợp chất của ng tố đó với hiđro Giúp mình với ạ...
1 câu trả lời
Đáp án:
CHe: $1s^2\ 2s^2\ 2p^6\ 3s^2\ 3p^4$ (2/8/6) ⇒ Z=16
a/ Vậy nguyên tố đó thuộc:
+) Ô số 16 (Z=16)
+) Chu kỳ 3 (vì có 3 lớp e)
+) Nhóm VIA (vì có nguyên tố p, 6 e lớp ngoài cùng)
⇒ Nguyên tố S (Lưu huỳnh).
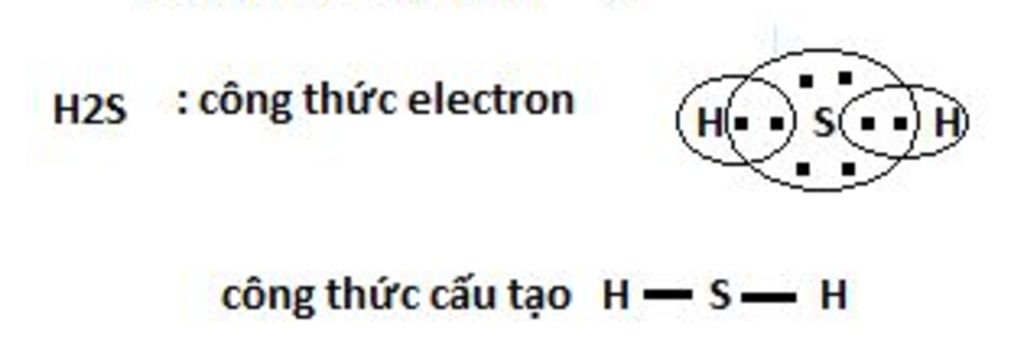
b/ Hợp chất của nguyên tố đó với hidro là: $H_2S$
Công thức e và công thức CT của $H_2S$ (Như hình vẽ)