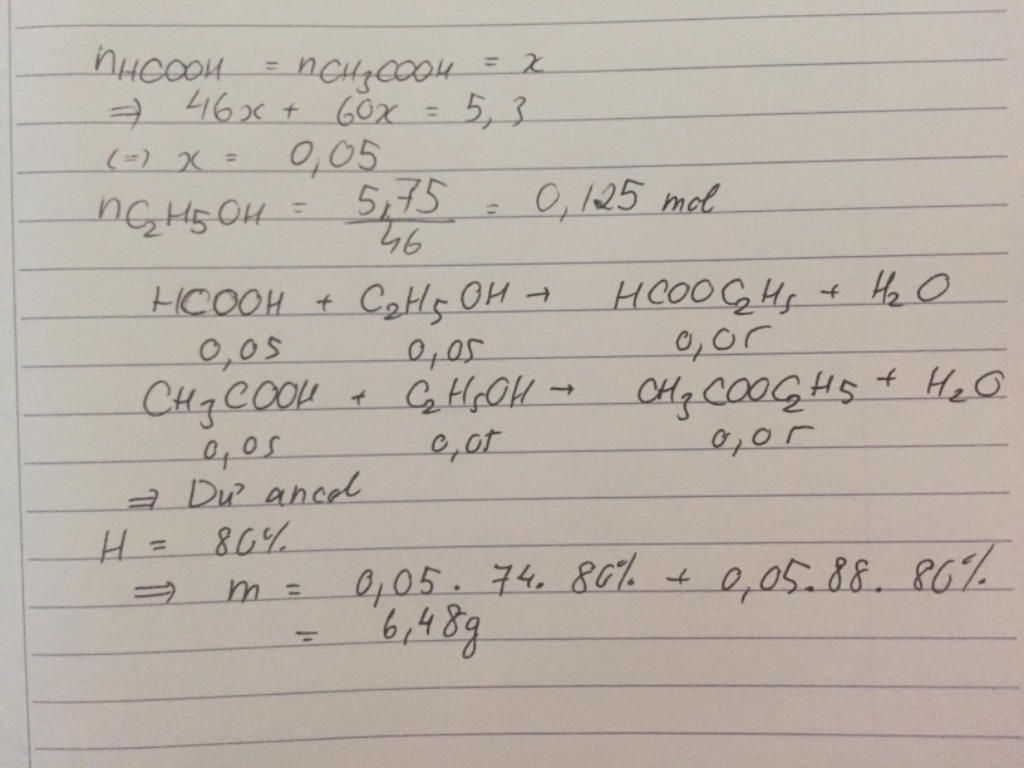Hỗn hợp X gồm axit HCOOH và CH3COOH (tỉ lệ mol 1:1). Lấy 5,3 gam hỗn hợp X tác với 5,75 gam CH3CH2OH (có xúc tác H2SO4 đặc) thu được m gam hỗn hợp este (hiệu suất của các phản ứng este hóa đều bằng 80%). Giá trị của m là: A. 10,12 B. 16,20 C. 6,48 D. 8,10
2 câu trả lời
Đáp án:
Theo đề ra ta có :
$m_{CH_3CH_2OH}$ `>` $m_{X}$ $\text{ ( Vì 5,75 > 5,3 ) }$
⇒ Sau phản ứng $m_{CH_3CH_2OH}$ dư , hỗn hợp X hết .
Đặt $CTTQ$ của `HCOOH` và `CH_3``COOH` là `RCOOH`
Ta có :
⇒ `n_(RCOOH)` = $\dfrac{5,3}{46 + 60}$ `×` `2` `=` `0,1` `mol`
⇒ $n_{CH_2CH_3OH}$ = `0,125` `mol`
Vì hỗn hợp `X` gồm axit `HCOOH` và `CH_3``COOH` có tỉ lệ mol `1` `:` `1`
`R` = $\dfrac{M_H + M_{CH_3} }{1 + 1}$ = $\dfrac{15 + 1}{2}$ = `8`
$m_{este}$ `=` `0,1` `.` `80``%` = `0,08`
→ $m_{RCOOHCH_2CH_3}$ = `0,08` . $\text{(8 + 44 + 29 )}$ = `6,48` `g`
$\text{Vậy chọn C}$
Câu hỏi trong lớp
Xem thêm