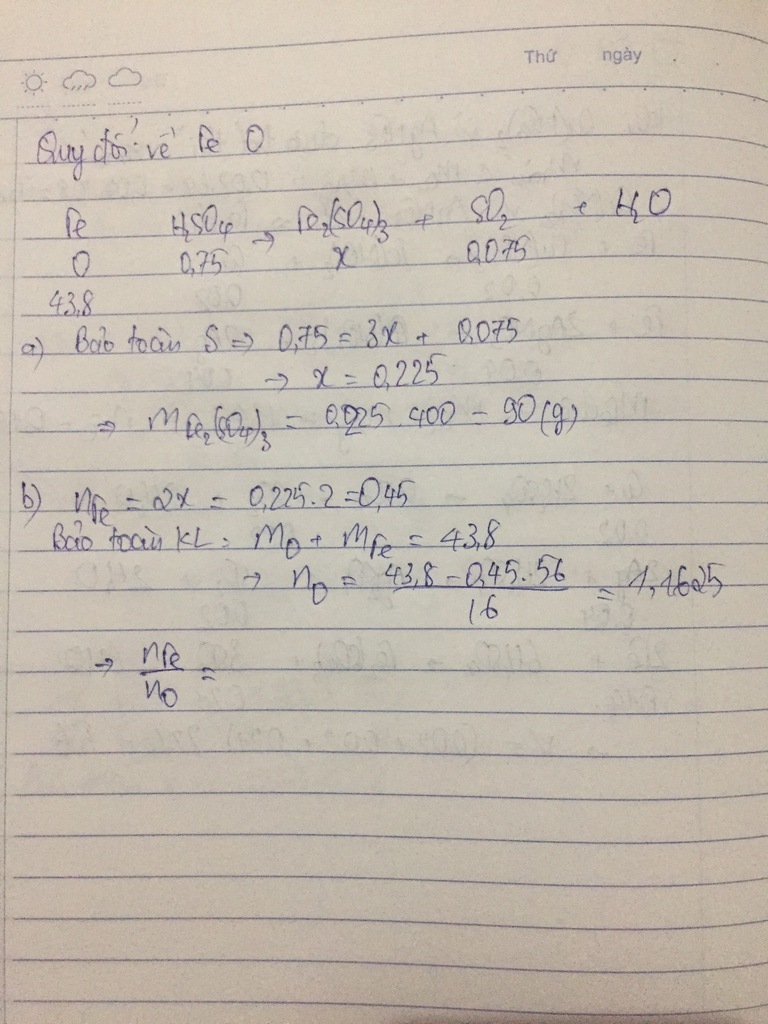Hòa tan 43,8gam một oxit sắt trong một lượng vừa đủ 75gam dung dịch H2SO4 98% thu được dung dịch chỉ chứa muối Fe2(SO4)3 và 1,68 lít khí SO2( đktc) a, tính khối lượng muối Fe2(SO4)3 thu được b, xác định công thức oxit sắt
2 câu trả lời
Đáp án:
Giải thích các bước giải:
mH2SO4 = 75.98% = 73,5 gam => nH2SO4 = 73,5/98 = 0,75 mol
nSO2 = 0,075 mol
a. BTNT "S": nH2SO4 = 3.nFe2(SO4)3 + nSO2 => 0,75 = 3.nFe2(SO4)3 + 0,075
=> nFe2(SO4)3 = 0,225 mol
=> mFe2(SO4)3 = 0,225.400 = 90 gam
b. BTNT "Fe": nFe = 2nFe2(SO4)3 = 0,45 mol
=> mO = m oxit - mFe = 43,8 - 0,45.56 = 18,6 gam
=> nO = 18,6 : 16 = 1,1625 mol
=> Fe : O = 0,45 : 1,1625 không thỏa mãn
Bạn xem lại đề bài nhé!