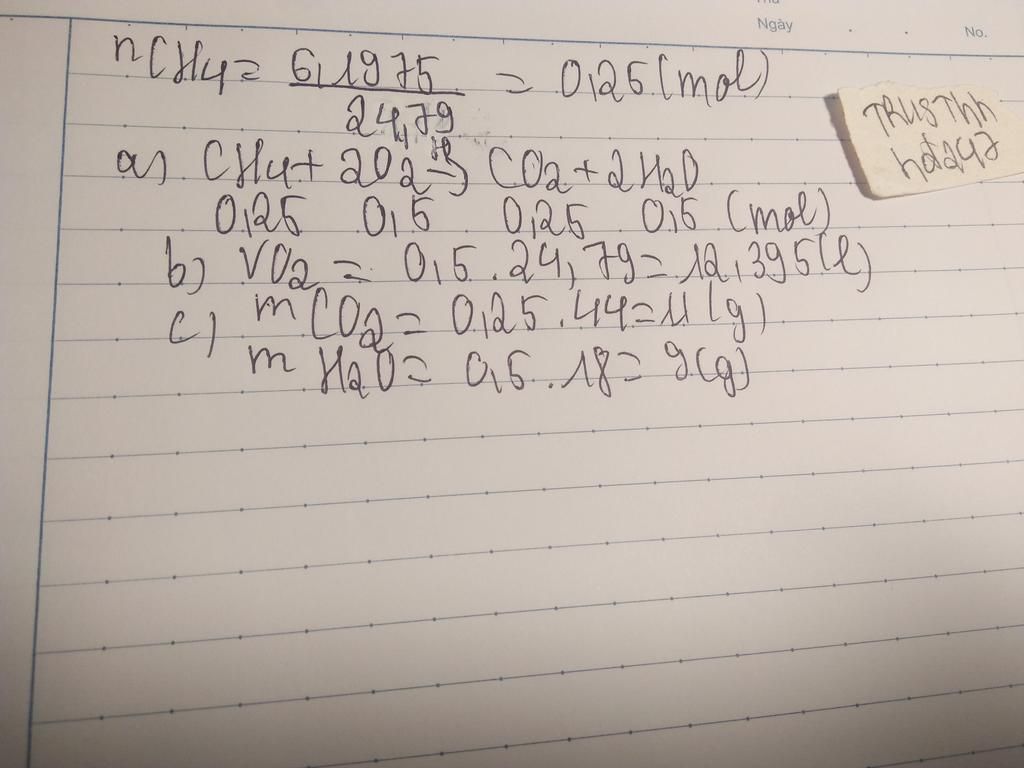Đốt cháy hoàn toàn 6,1975 lít khí methane (đkc) trong khí oxygen A.Viết pthh xảy ra B. Tính thể tích khí oxygen cần dùng C. Tính khối lượng sản phẩm thu được sau phản ứng
2 câu trả lời
Đáp án
$a)CH_4+2O_2\xrightarrow{t^o}CO_2+2H_2O$
$b)V_{O_2}=12,395(lít)$
$c)m_{CO_2}=11(g);m_{H_2O}=9(g)$
Giải thích các bước giải:
$a)PTHH:CH_4+2O_2\xrightarrow{t^o}CO_2+2H_2O$
$b)n_{CH_4}=\dfrac{6,1975}{24,79}=0,25(mol)$
Theo PT: $n_{O_2}=2n_{CH_4}=0,5(mol)$
$\Rightarrow V_{O_2(đkc)}=0,5.24,79=12,395(lít)$
$c)$ Theo PT: $n_{CO_2}=n_{CH_4}=0,25(mol);n_{H_2O}=n_{O_2}=0,5(mol)$
$\Rightarrow m_{CO_2}=0,25.44=11(g);m_{H_2O}=0,5.18=9(g)$
Câu hỏi trong lớp
Xem thêm