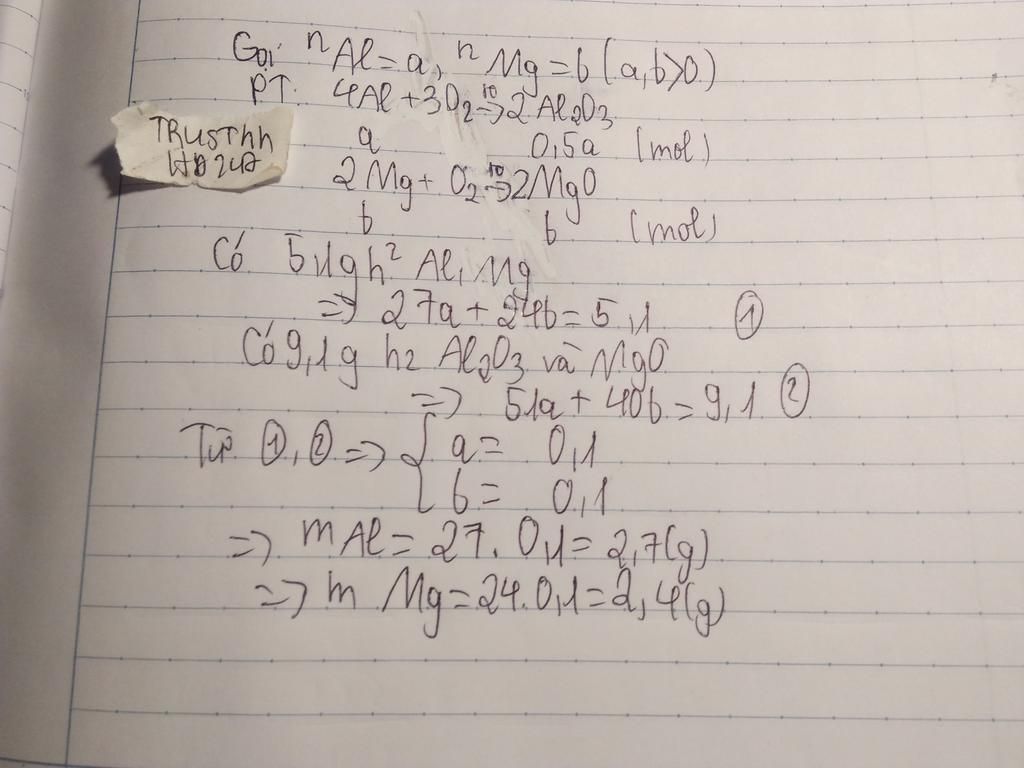Đốt cháy hoàn toàn 5,1 gam hỗn hợp kim loại Al và Mg trong bình chứa khí O2 vừa đủ thu được 9,1 gam hỗn hợp oxit Al2O3 và MgO. Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu.
2 câu trả lời
Đáp án:
`↓`
Giải thích các bước giải:
Áp dụng ĐLBTKL, ta có:
`m_{hh kl}``+``m_{O_2}``=``m_{oxit}`
`⇔``5,1``+``M_{O_2}``=``9,1`
`⇔``m_{O_2}``=``4` `(g)`
`n_{O_2}``=``\frac{m}{M}``=``\frac{4}{32}``=``0,125` `(mol)`
Gọi `x``,` `y` lần lượt là số mol của `Al` và `Mg` `(``x``,` `y``>``0``)`
`4Al``+``3O_2` $\xrightarrow[]{t^o}$ `2Al_2O_3` `(1)`
`x` `0,75x` `mol`
`2Mg``+``O_2` $\xrightarrow[]{t^o}$ `2MgO` `(2)`
`y` `0,5y` `mol`
Theo đề bài và pt `(1)``,` `(2)` ta có hpt:
$\left \{ {{27x+24y=5,1} \atop {0,75x+0,5y=0,125}} \right.$`⇒`$\left \{ {{x=0,1} \atop {y=0,1}} \right.$
`→``m_{Al}``=``n``.``M``=``0,1``.``27``=``2,7` `(g)`
`→``m_{Mg}``=``m_{hh kl}``-``m_{Al}``=``5,1``-``2,7``=``2,4` `(g)`