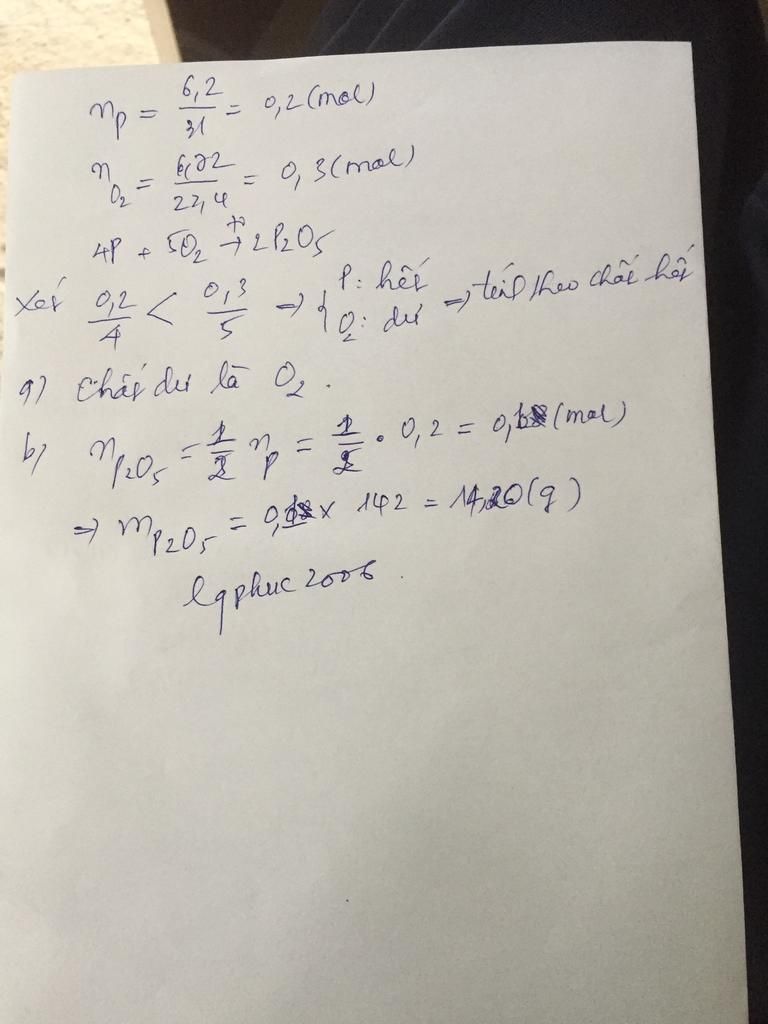Đốt cháy 6,2g P đỏ trong bình chứa 6,72 lít khí Oxi (ở đktc) tạo thành P2O5 a: chất nào còn dư b: khối lượng chất tạo thành là bao nhiêu
2 câu trả lời
`a,` `n_P``=``\frac{m}{M}``=``\frac{6,2}{31}``=``0,2` `(mol)`
$n_{O_2(đktc)}$`=``\frac{V}{22,4}``=``\frac{6,72}{22,4}``=``0,3` `(mol)`
`4P``+``5O_2` $\xrightarrow[]{t^o}$ `2P_2``O_5`
Ban đầu `0,2` `0,3` `mol`
Trong pứng `0,2` `0,25` `0,1` `mol`
Sau pứng `0` `0,05` `0,1` `mol`
Sau phản ứng `O_2` còn dư
`b,`Theo pt, ta có: `n_{P_2O_5}``=``n_P``=``\frac{0,2.2}{4}``=``0,1` `(mol)`
`→``m_{P_2O_5}``=``n``.``M``=``0,1``.``142``=``14,2` `(g)`