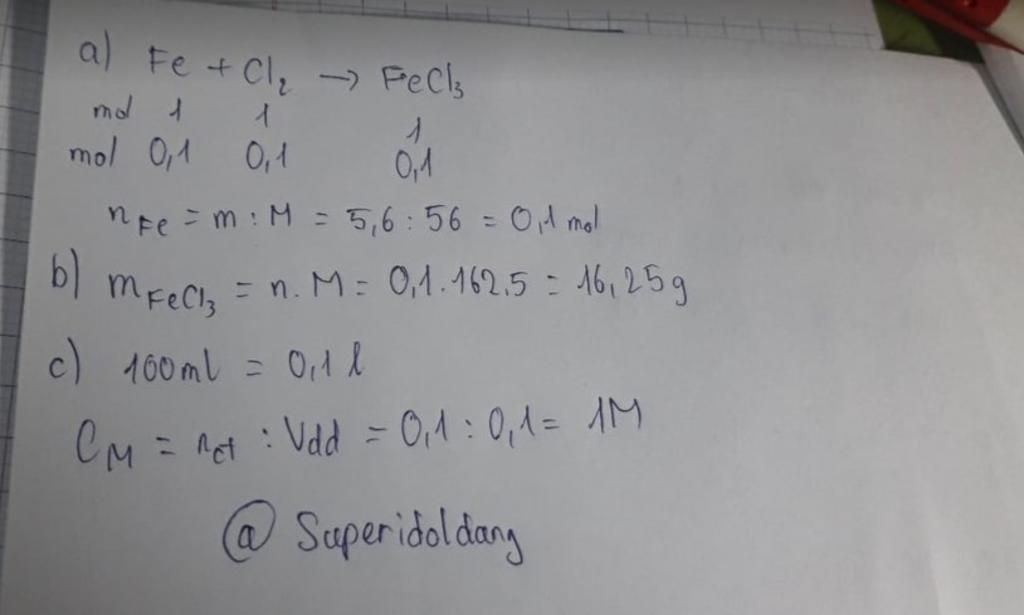Đốt cháy 5,6 g fe trong khí clo dư. a. Viết phương trình hóa học xảy ra b. Tính khối lượng muối tạo thành c. Hòa tan lượng muối trên bằng 100ml nước. Tính nồng độ mol của dung dịch thu được?
2 câu trả lời
$\text{#Festival :🎁}$
$\text{n$_{Fe}$=5,6:56=0,1(mol)}$
$\text{a,PTHH:}$
$\text{2Fe+3Cl$_{2}$→2FeCl$_{3}$}$
$\text{0,1 → 0,1 (mol)}$
$\text{b, Từ PTHH ta suy ra : n$_{FeCl3}$=0,1(mol)}$
$\text{⇒m$_{FeCl3}$=0,1.162,5=16,25(g)}$
$\text{c,Nồng độ mol :}$
$\text{C$_{M FeCl3}$=$\frac{0,1}{0,1}$ =1(M)}$