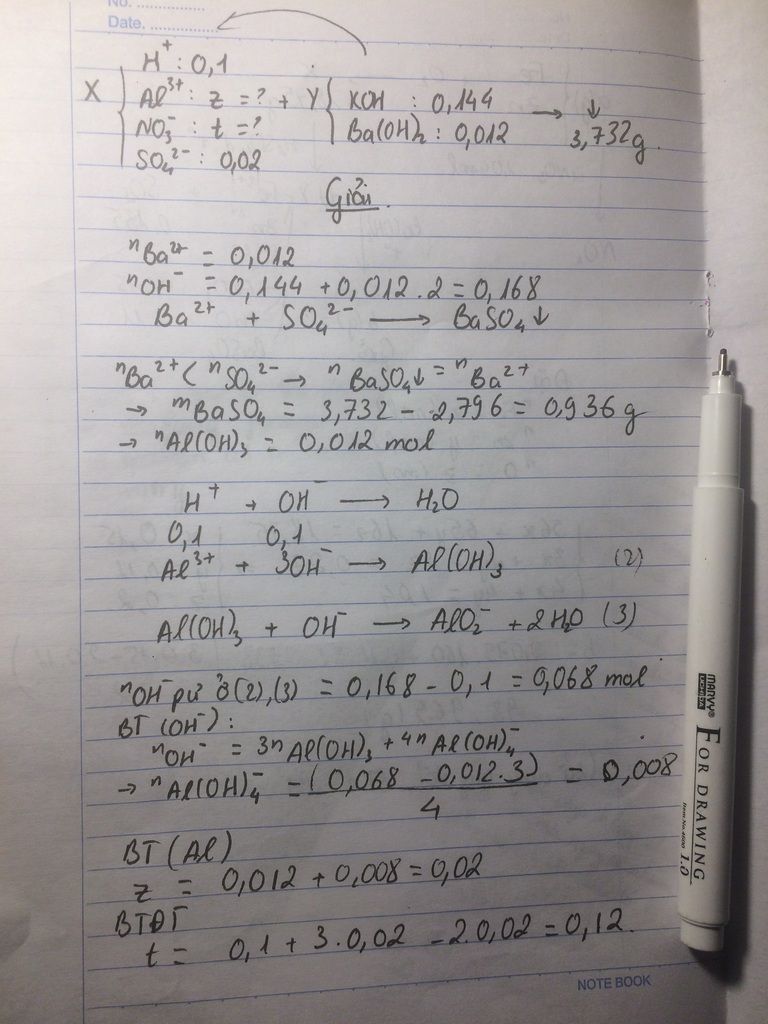DdX gồm 0,1mol H+ ,z mol Al3+,t mol NO3_ và 0,02mol SO42-.cho 120ml ddY gồm KOH 1,2M và Ba(OH)2 0,1M vào X sau khi các p.ư kết thúc thu đưojc 3,732g kết tủa.tính z,t
2 câu trả lời
$n_{KOH}$ = 0,144 mol; $n_{Ba(OH)_{3}}$ = 0,012 mol
$n_{OH^{-}}$ = 0,144 + 0,012.2 = 0,168 mol
$H^{+}$ + $OH^{-}$ → H2O
0,1 0,168
⇒ $n_{OH-}$ dư = 0,168 - 0,1 = 0,068 mol
$Ba^{2+}$ + $SO4^{2-}$ → BaSO4↓
0,012 0,02 0,012
$Al^{3+}$ + 3$OH^{-}$ → Al(OH)3↓
3,732 g ↓ chứa BaSO4 và Al(OH)3
⇒ $m_{BaSO4}$ + $m_{Al(OH)3}$ = 3,732 g
⇒ $m_{Al(OH)3}$ = 3,732 - $m_{BaSO4}$ = 3,732 - 0,012.233 = 0,936 g
⇒ $n_{Al(OH)3}$ = 0,012 mol
$Al^{3+}$ + 3$OH^{-}$ → Al(OH)3
Al(OH)3 + $OH^{-}$ → $Al(OH)4^{-}$
$n_{OH-}$ dư = 0,068 = 3.$n_{Al(OH)3}$ + 4.$n_{Al(OH)4^{-}}$
⇒ $n_{Al(OH)4^{-}}$ = (0,068 - 3.0,012) : 4 = 0.008 mol
Bảo toàn Al ta có $n_{Al³+}$ = $n_{Al(OH)3}$ + $n_{Al(OH)4^{-}}$ = z = 0,012 + 0,008 = 0,02
Bảo toàn điện tích trong dd X ta có
.$n_{H+}$ + 3.$n_{Al³+}$ = $n_{NO3-}$ + 2.$n_{SO4²-}$
⇔ 0,1 + 3.0,02 = t + 2.0,02
⇔ t = 0,12
Vậy z = 0,02 và t = 0,12