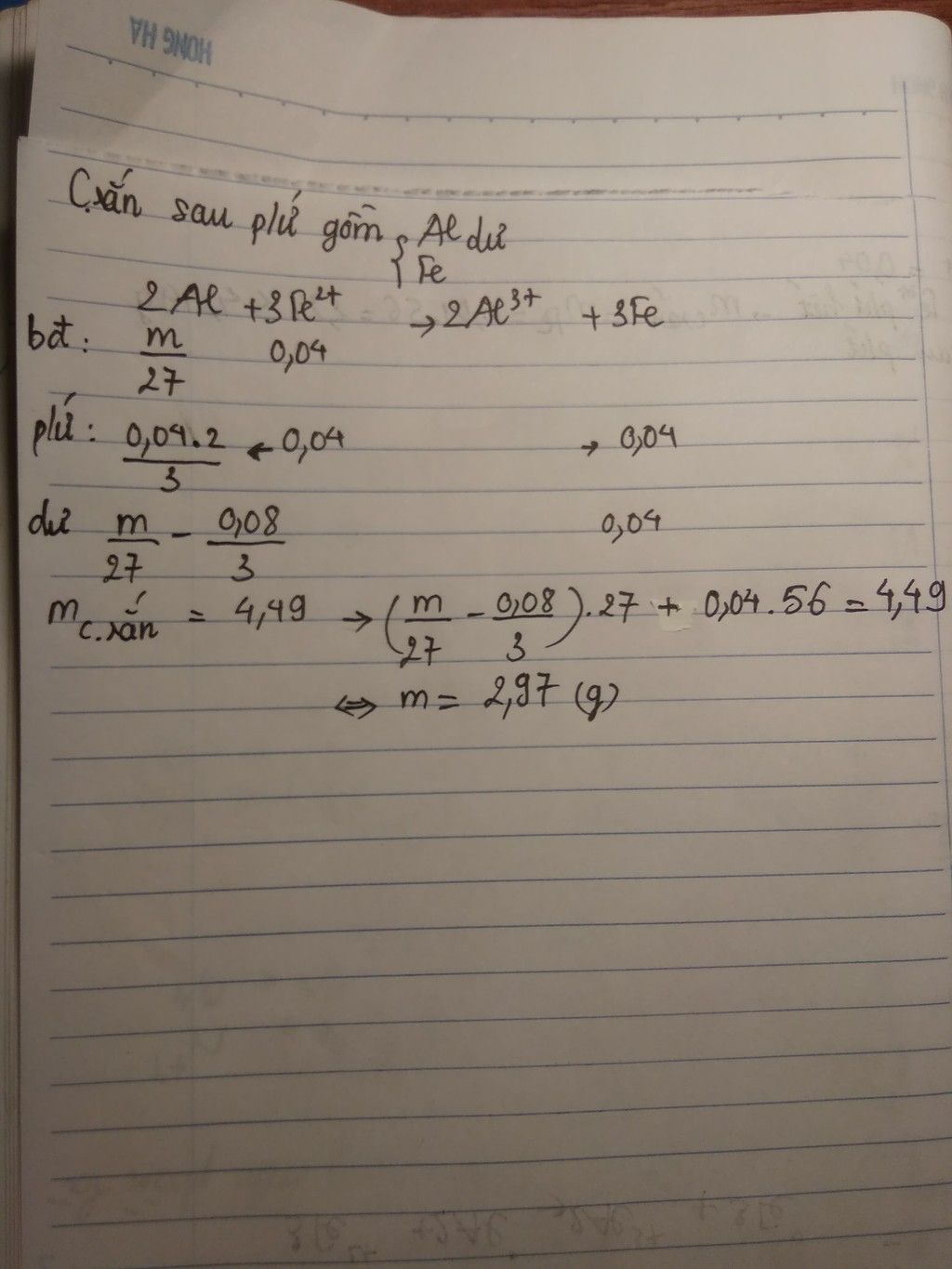Cho m gam Al vào 200ml dd Fe(NO3)2 0,2M đến khi pứ xảy ra hoàn toàn, thu được 4,49 gam chất rắn. Giá trị của m là
2 câu trả lời
Đáp án:
m = 2,97
Giải thích các bước giải:
nFe(NO3)2 = 0,2 . 0,2 = 0,04 mol
2Al + 3Fe(NO3)2 → 2Al(NO3)3 + 3Fe
Giả sử Al phản ứng hết
nFe = nFe(NO3)2 phản ứng ≤ 0,04
→ mFe ≤ 0,04 . 56 = 2,24g < 4,49
→ Fe(NO3)2 phản ứng hết, chất rắn thu được có Al và Fe còn dư
mAl dư = 4,49 - 2,24 = 2,25g
nAl p.ư = 2/3nFe(NO3)2 = 0,08/3
m = 2,25 + 0,08/3 . 27 = 2,97g
Câu hỏi trong lớp
Xem thêm