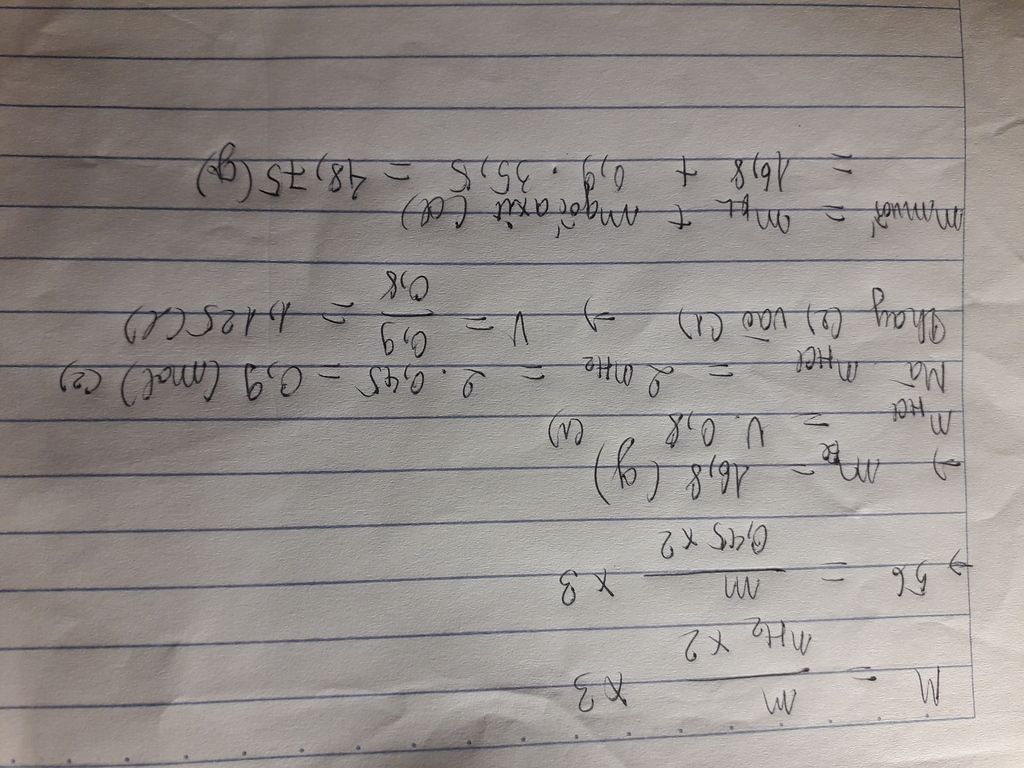Cho a gam Fe tác dụng với dung dịch HCl 0,8M. Sau phản ứng thu được 10,08 lít khí H2 đktc. Tính a gam và thể tích dd HCl cần dùng ? Và khối lượng muối tạo thành. ( không viết pthh, áp dụng định luật bào toàn electron để giải)
2 câu trả lời
$n_{H_2}=\frac{10,08}{22,4}=0,45(mol)=>n_{H}=0,45.2=0,9(mol)$
$Fe → Fe^{2+}+2e $
0,45 ← 0,9
$H^{+}+1e → H$
0,9 0,9←0,9
$m_{Fe}=0,45.56=25,2(g)$
$n_{HCl}=n_{Cl}=n_{H}=0,9(mol)$
$V_{HCl}=\frac{n_{HCl}}{C_{M_HCl}}=\frac{0,9}{0,8}=1,125(l)$
$m_{muối}=m_{Fe}+m_{Cl}=25,2+0,9.35,5=57,15(g)$