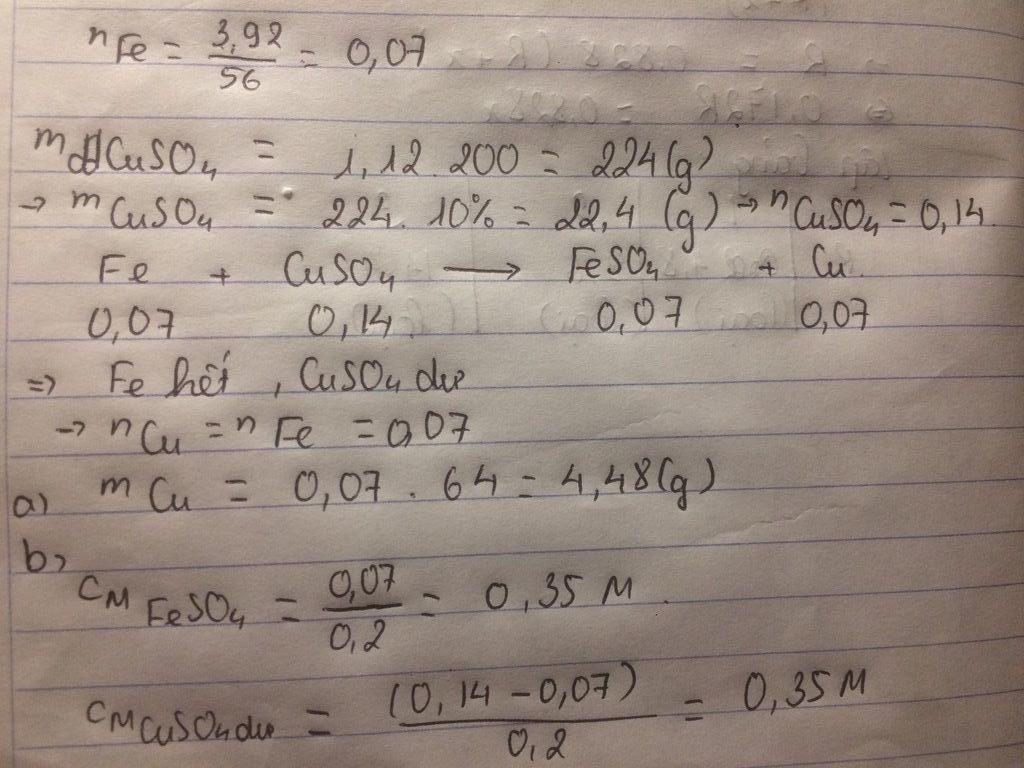Cho 3,92g bột sắt vào 200ml dd cuso4 10% (Đ = 1.12 g /mml) a) tính khối lượng kim loại mới tạo thành b) tính nồng độ mol của chất có trong dd sau phản ứng
2 câu trả lời
Đáp án:
a, 4,48g
b, $\matrix{
{{C_{M(FeS{O_4})}} = 0,35(M)} \hfill \cr
{{C_{M(CuS{O_4})}} = 0,35(M)} \hfill \cr }$
Giải thích các bước giải:
mddCuSO4 = 200 . 1,12 = 224g
→ mCuSO4 = 224 . 10% = 22,4g
→ nCuSO4 = 22,4 : 160 = 0,14mol
nFe = 3,92 : 56 = 0,07 mol
Fe + CuSO4 → FeSO4 + Cu
nFe < nCuSO4 → Fe phản ứng hết, CuSO4 dư
nCu = nFe = 0,07 mol
→ mCu = 0,07 . 64 = 4,48g
Sau phản ứng thu được dung dịch gồm:
FeSO4: nFeSO4 = nFe = 0,07 mol
CuSO4 dư: nCuSO4 p.ứ = nFe = 0,07 mol → nCuSO4 dư = 0,14 - 0,07 = 0,07 mol
$\matrix{
{{C_{M(FeS{O_4})}} = {{0,07} \over {0,2}} = 0,35(M)} \hfill \cr
{{C_{M(CuS{O_4})}} = {{0,07} \over {0,2}} = 0,35(M)} \hfill \cr }$