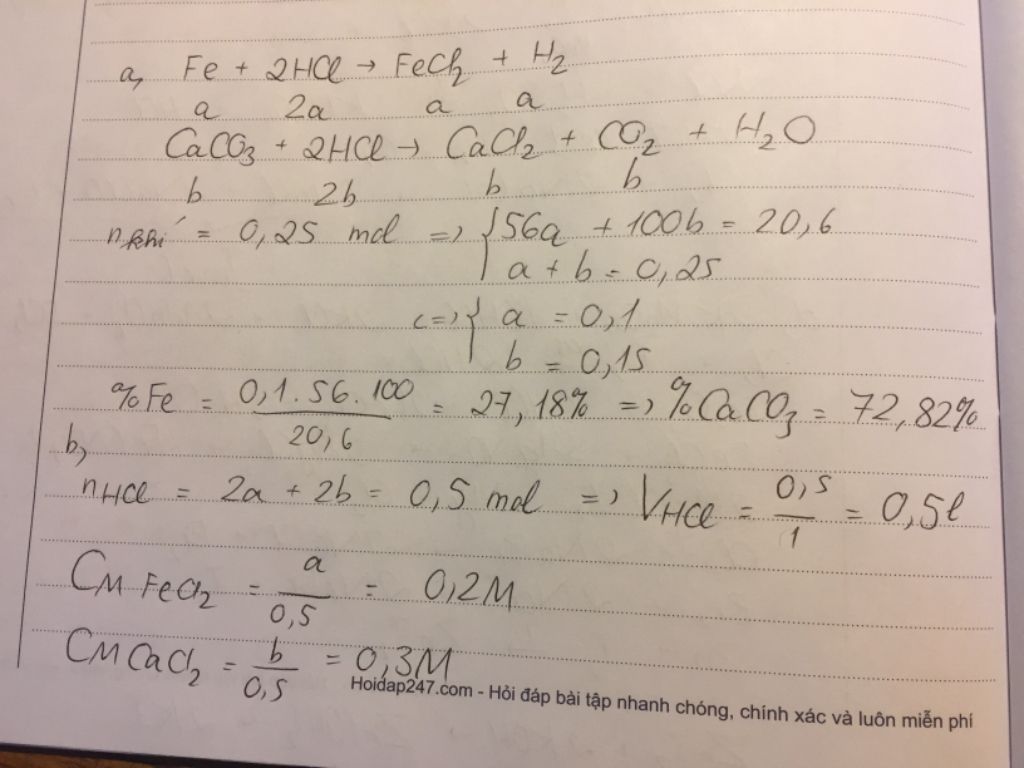: Cho 20,6 gam hỗn hợp gồm Fe và CaCO3 tác dụng vừa đủ với dung dịch HCl 1M. Sau khi phản ứng kết thức thu được dung dịch A và 5,6 lít hỗn hợp khí (đktc). a/. Tính phần trăm khối lượng mỗi chất trong hỗn hợp ban đầu? b/. Tính nồng độ mol các chất có trong dung dịch A? Giả sử thể tích dung dịch thay đổi không đáng
2 câu trả lời
Đáp án:a)
%Fe= 27,18%
% CaCO3=15%
b)
CMFeCl2=0,2 (mol/l)
CMCaCl2=0,3 (mol/l)
Giải thích các bước giải:Gọi a và b lần lượt là số mol của Fe và CaCO3
Fe + 2HCl--> FeCl2 +H2
a 2a a a
CaCO3 + 2HCl---> CaCl2 + H2O +CO2
b 2b b b b
n khí= a+b=5,6/22,4=0,25 (mol)
n hh= 56a + 100b=20,6 (g)
==> a=0,1;b=0,15
m Fe= 56.0,1=5,6 (g)
mCaCO3=100.0,15=15 (g)
%Fe= (5,6/20,6).100%=27,18%
% CaCO3=( 15/100).100%=15%
VHCl=n/CM=(2a+2b)/1=0,2+0,3=0,5(l)
thể tích trong dd thay đổi không đáng kể--> VddA= 0,5(l)
sau phản ứng thu đc dd A gồm dd FeCl2 và CaCl2
CMFeCl2=0,1/0,5=0,2 (mol/l)
CMCaCl2=0,15/0,5=0,3 (mol/l)
Câu hỏi trong lớp
Xem thêm