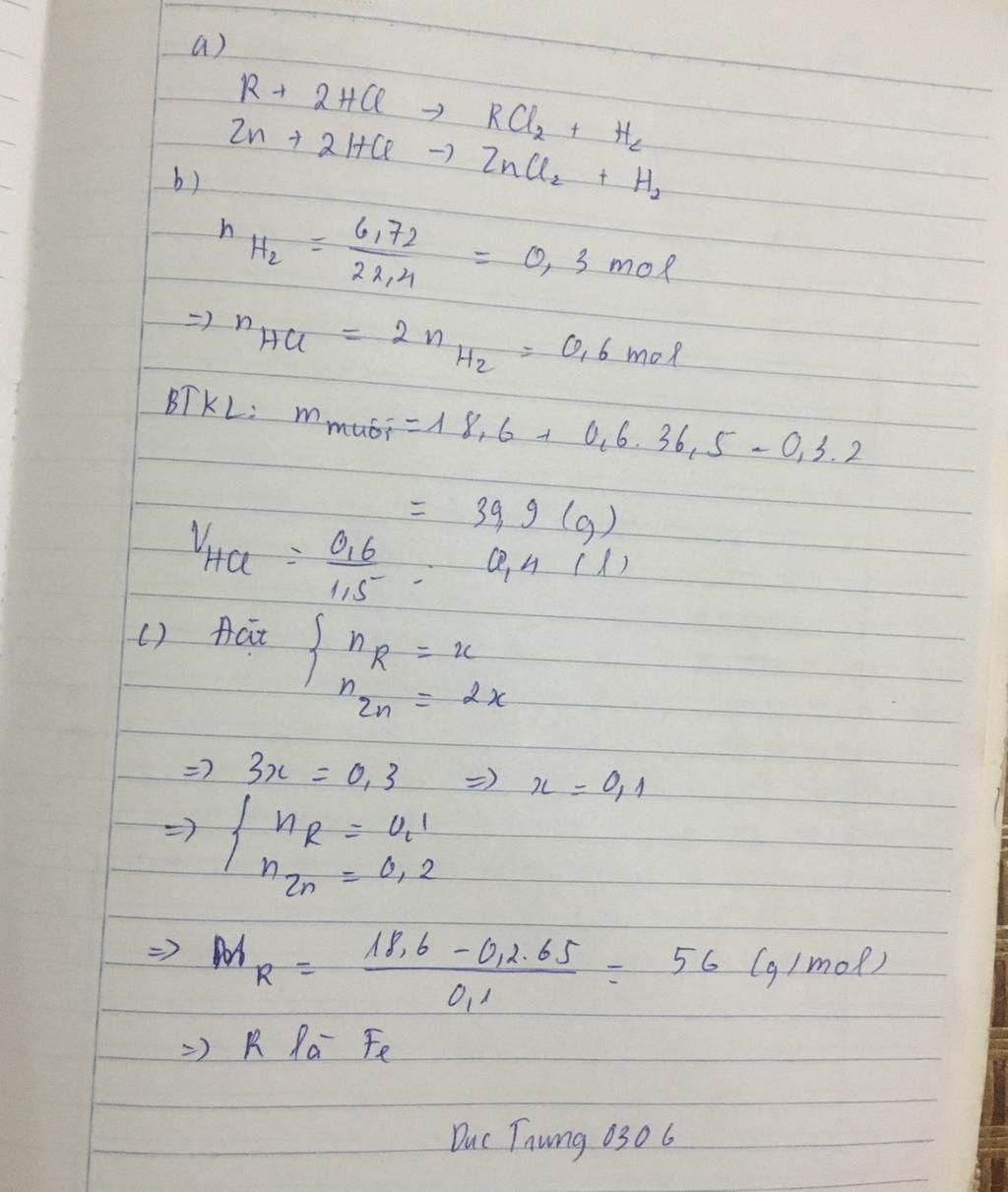Cho 18,6 gam hỗn hợp 2 kim loại là R có hoá trị II và Zn tác dụng với dung dịch HCl dư. Khi phản ứng kết thúc thu được dung dịch 2 muối và 6,72 lít khí (ở đktc). Biết rằng trong hỗn hợp ban đầu tỉ lệ số mol R : Zn là 1 : a) Viết các phương trình phản ứng đã xảy ra. b) Tính khối lượng mỗi muối thu được sau phản ứng và tính thể tích dung dịch HCl 1,5M tối thiểu cần dùng. c) Xác định kim loại R
2 câu trả lời
Đáp án:
Giải thích các bước giải:
a)
$ R + 2HCl → RCl_2 + H_2 $
$Zn + 2HCl → ZnCl_2 + H_2$
b
$n_{H_2}$ = $\frac{6,72}{22,4}$ = 0,3 mol
Bảo toàn nguyên tố $H$:
$n_{HCl} = 2n_{H_2} = 0,6 mol$
→ `n_{Cl}` = 0,6 mol
Theo bảo toàn khối lượng:
`m` muối = `m` kim loại + `m_{Cl^-}`
$ = 18,6 + 0,6 . 35,5 =39,9g $
`V_{HCl}` = $\frac{0,6}{1,5}$ = 0,4`l`
c)
Ta có:
`n` kim loại = `n_{H_2}` = 0,3 mol
Gọi số mol `Zn, R` là `x` và `y`
Ta có `x` + `y` = 0,3
Mà `x` : `y` = 1 : 2
→ `x` = 0,2 `y` = 0,1
`m_R` = 18,6 - 0,2 . 65 = 5,6g
`M_R` = $\frac{5,6}{0,1}$ = 56 g/mol
Vậy R là Fe
Chúc bạn học tốt #aura