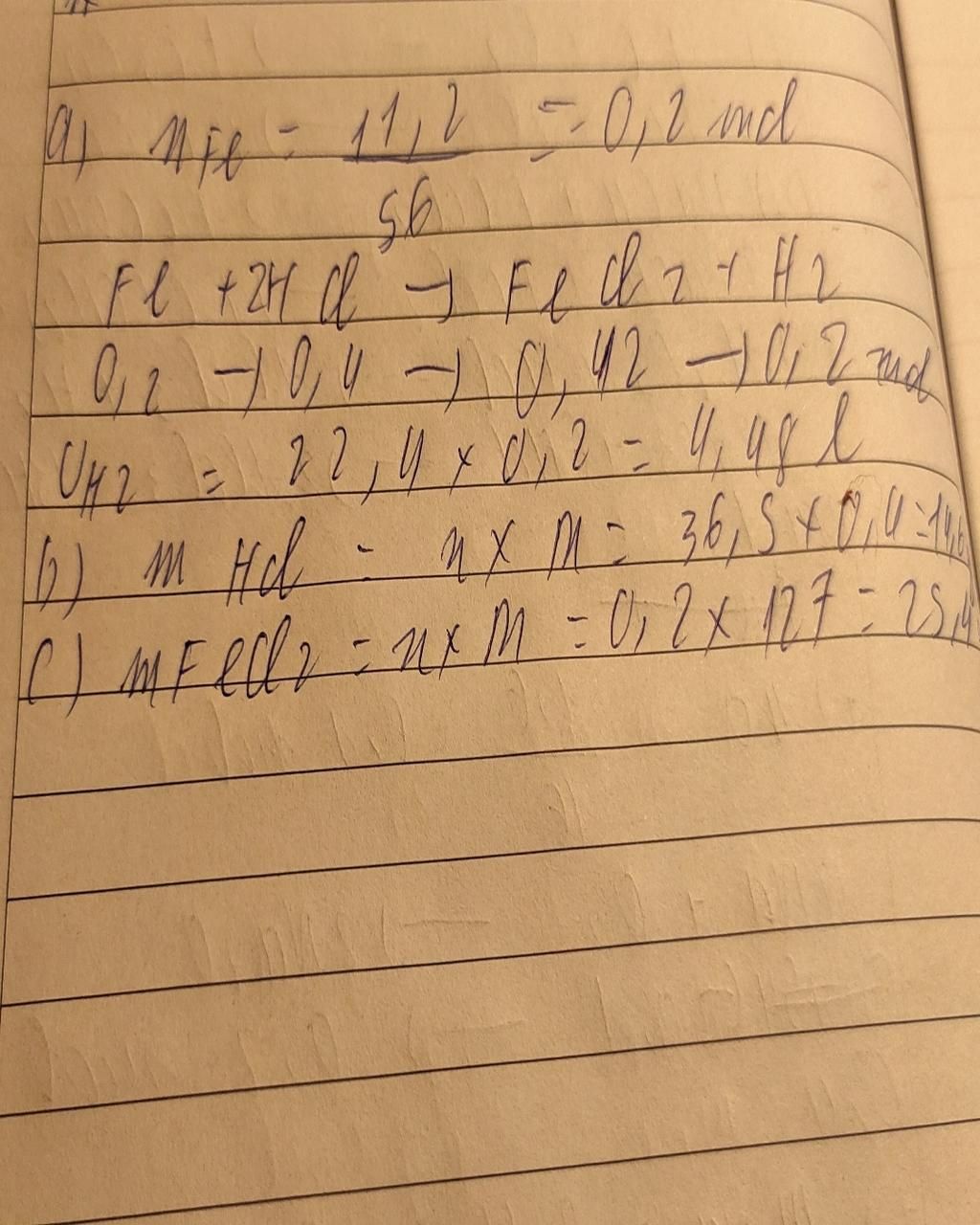Cho 11,2 gam Fe tác dụng với dung dịch HCL. Tính a, Thể tích khí H2 thu đc ở đktc b, Khối lượng HCL phản ứng c, Khối lượng FeCl2 tạo thành
2 câu trả lời
Giải thích các bước giải:
$n_{Fe}=$ `(11,2)/(56)` $=0,2mol$
PTHH:
$Fe+2HCl→FeCl_2+H_2↑$
0,2 0,4 0,2 0,2 (mol)
a/.
Theo phương trình, ta có:
$n_{H_2}=n_{Fe}=0,2mol$
$V_{H_2(đktc)}=0,2.22,4=4,48 lít$
b/.
Ta có:
$n_{HCl}=2.n_{Fe}=2.0,2=0,4mol$
$m_{HCl}=0,4.36,5=14,6g$
c/.
Ta có:
$n_{FeCl_2}=n_{Fe}=0,2mol$
$m_{FeCl_2}=0,2.127=25,4g$
Câu hỏi trong lớp
Xem thêm