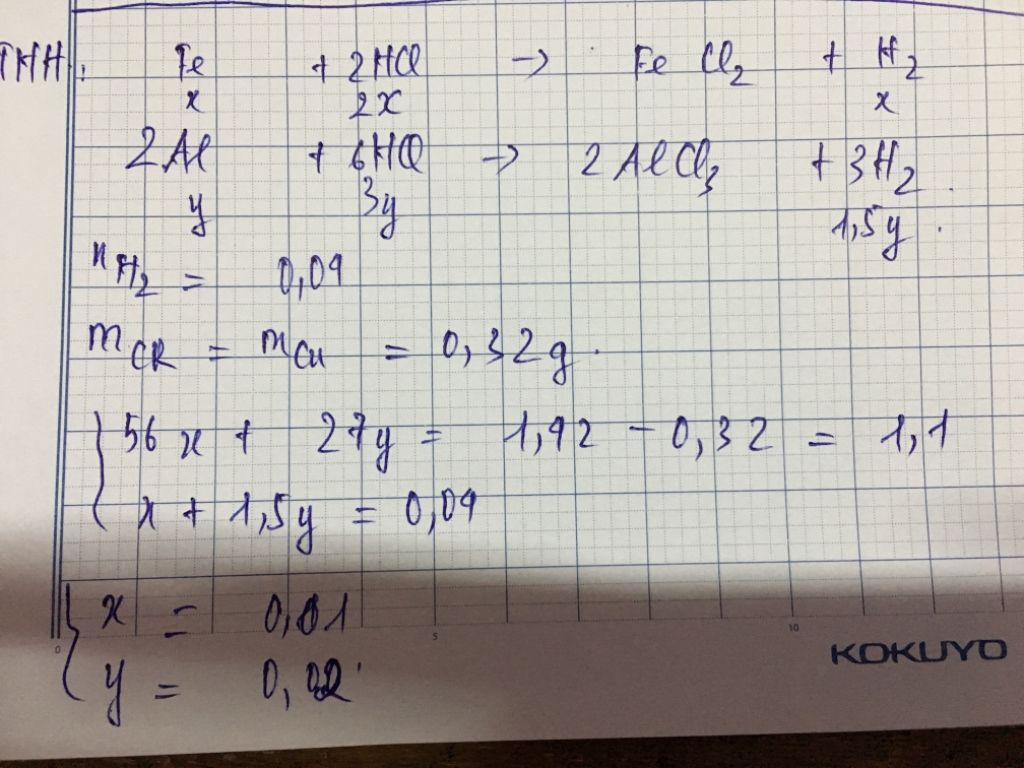Cho 1,42 g hh (Fe,Al,và Cu) vào dung dịch HCl thấy thoát ra 896 ml khí H2(đktc) và 0,32 g một chất rắn không tan. Viết pt hóa học của các pư xảy ra? Tính thành phần phần trăm về khối lượng của mỗi kim loại trong hh ban đầu? Tính thể tích HCl 0,1M đủ để hòa tan hh trên
2 câu trả lời
Đáp án:
%mFe=39,44%; %mAl=38,03% -> %mCu=22,53%
V HCl=0,8 lít
Giải thích các bước giải:
Cu không phản ứng với HCl.
Fe + 2HCl ---> FeCl2 + H2
Al + 3HCl ---> AlCl3 + 3/2 H2
-> mCu=0,32 gam
Gọi số mol Fe là x; Al là y -> 56x+27y=1,42-0,32=1,1 gam
nH2=x+1,5y=0,896/22,4=0,04 mol
Giải được: x=0,01; y=0,02
-> mFe=0,01.56=0,56 gam; mAl=0,02.27=0,54 mol
->%mFe=39,44%; %mAl=38,03% -> %mCu=22,53%
nHCl=2nH2=0,08 mol -> V HCl=0,08/0,1=0,8 lít
Câu hỏi trong lớp
Xem thêm