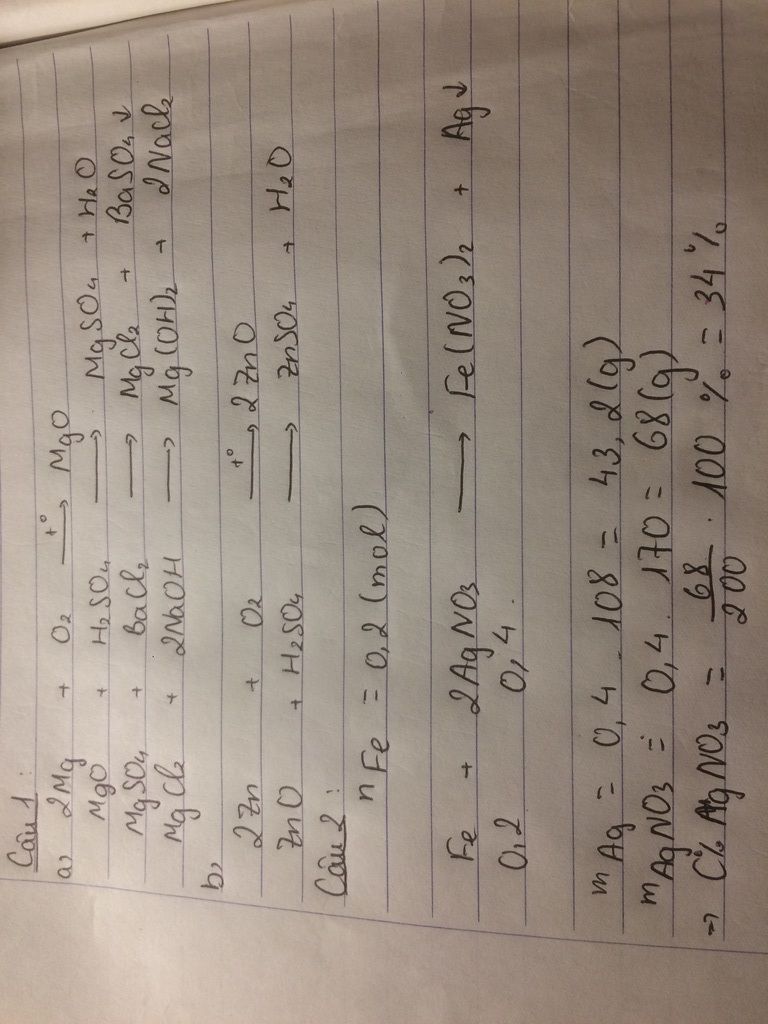Câu1 Viết phương trình phản ứng thực hiện chuỗi biến đổi hoá học sau a, Mg -¹> MgO-²> MgSO4-³> MgCl2-⁴> Mg(OH)2 b, Zn-¹> ZnO-²> ZnSO4-³> MgCl2-⁴> Mg(OH)2 Câu 2 hoà tan hoàn toàn 11,2g Fe vào 200ml dd AgNO3 . Sau pư thu được chất rắn màu trắng bạc a, viết phương trình phản ứng b, tính khối lượng chất rắn thu được c, tính nồng độ mol của dd AgNO3 đã dùng (Biết Ag=108 , Fe=56 , N=14 , Ở=16)
2 câu trả lời
Câu 1:
a) 2Mg + O2 -> 2MgO
MgO + H2SO4 -> MgSO4 + H2O
MgSO4 + BaCl2 -> MgCl2 + BaSO4
MgCl2 + NaOH -> Mg(OH)2 + NaCl
b) Tương tự như trên :')
Câu 2:
a) Fe + 2AgNO3 -> Fe(NO3)2 + 2Ag
0,2 0,4 0,2 0,4 (mol)
nFe = 11,2/56 = 0,2 mol
mAg = 0,4. 108 = 43,2g
mctAgNO3 = 0,4 . 170 = 68g
=> C% AgNO3 = 68/200 . 100 = 34%