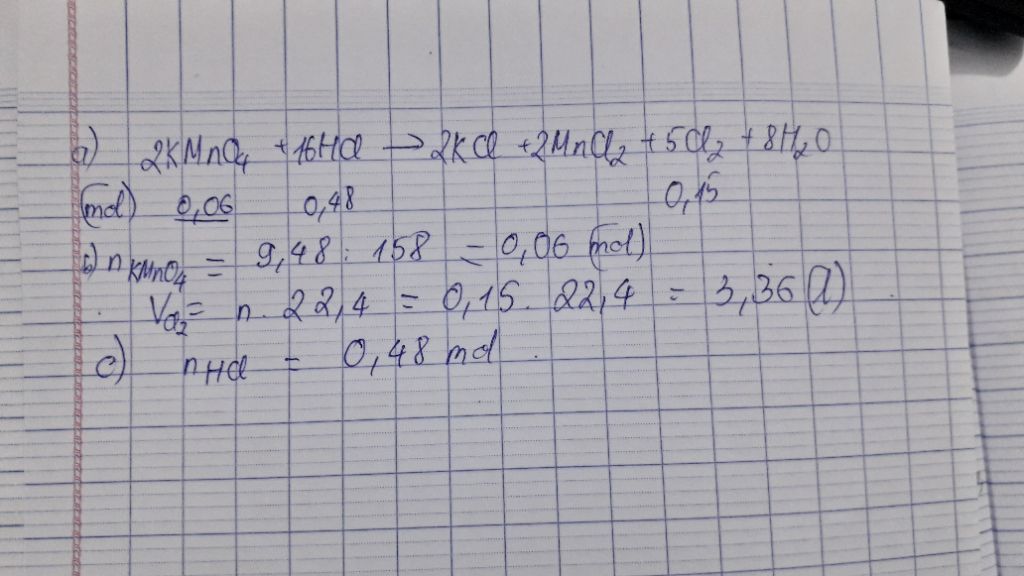Cần người giúp, hứa cảm ơn và vote 5 sao ạ Cho 9.48 gam KMnO4 tác dụng vừa đủ với dung dịch HCl tới khi phản ứng xảy ra hoàn toàn thu được V lít khí Cl2 (đktc) a) viết phương trình hóa học đã xảy ra và cân bằng b) tính V c) tính số mol HCl đã tham gia phản ứng
2 câu trả lời
Đáp án:
Giải thích các bước giải:
a)
\(2KMn{O_4} + 16HCl \to 2KCl + 2MnC{l_2} + 5C{l_2} + 8{H_2}O\)
\(\begin{array}{l}
b)\\
nKMn{O_4} = \frac{{9,48}}{{158}} = 0,06\,mol\\
= > nC{l_2} = 0,15\,mol\\
V = 0,15 \times 22,4 = 3,36\,l\\
c)\\
nHCl = \frac{{0,06 \times 16}}{2} = 0,48\,mol
\end{array}\)
Câu hỏi trong lớp
Xem thêm