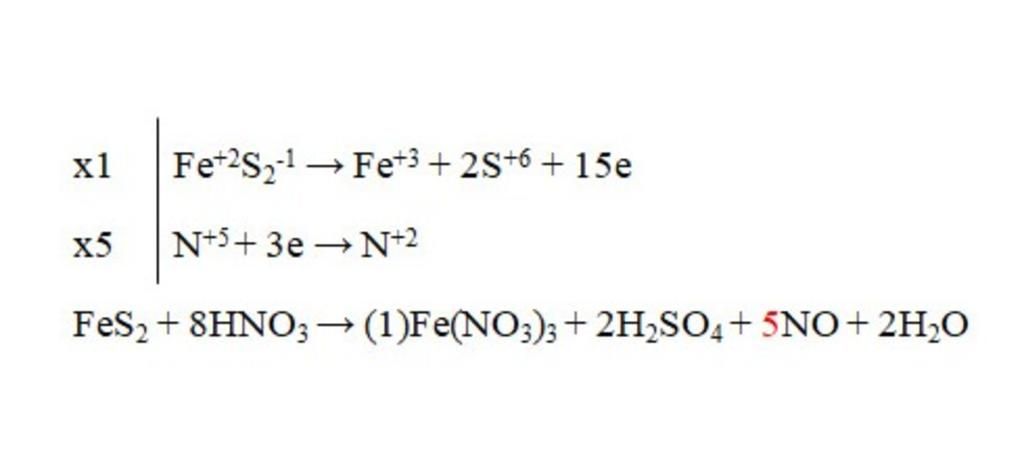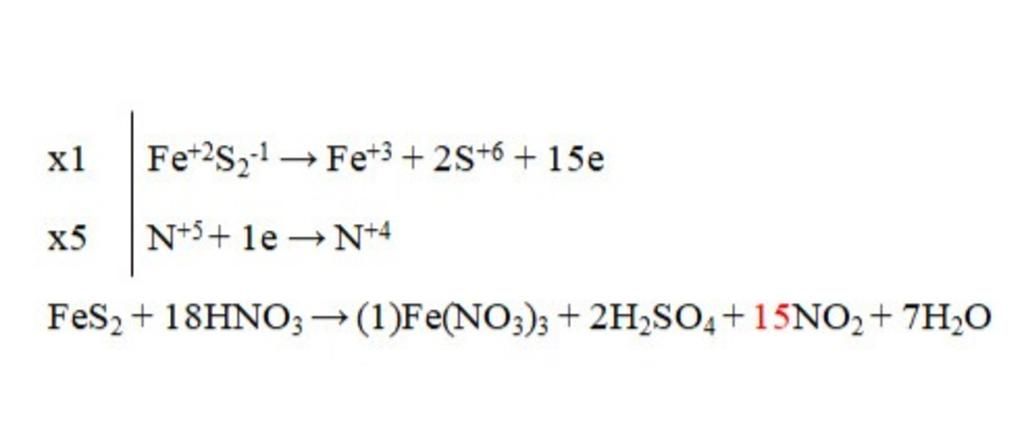cân bằng phản ứng oxi hóa khử FeS2+ HNO3 → Fe(NO3)3 + NO2+ H2O
2 câu trả lời
Giải thích các bước giải:
$Fe^{+2}S_2^{-1}+HN^{+5}O_3→Fe^{+3}(NO_3)_3+H_2S^{+6}O_4+N^{+4}O_2+H_2O$
+ Chất khử: $FeS_2$
+ Chất oxi hóa: $HNO_3$
$FeS_2$ nếu xét số oxi hóa từng chất thì hơi phức tạp, nên mình xét cả hợp chất $FeS_2$, số oxi hóa của hợp chất là $0$
$(FeS_2)^0+HN^{+5}O_3→Fe^{+3}(NO_3)_3+H_2S^{+6}O_4+N^{+4}O_2+H_2O$
+ Quá trình oxi hóa:
$1$ x $|FeS_2^0+15e→Fe^{+3}+2S^{+6}$
+ Quá trình khử:
$15$ x $|N^{+5}→N^{+4}+1e$
+ Cân bằng PT:
$FeS_2+18HNO_3→Fe(NO_3)_3+2H_2SO_4+15NO_2↑+7H_2O$