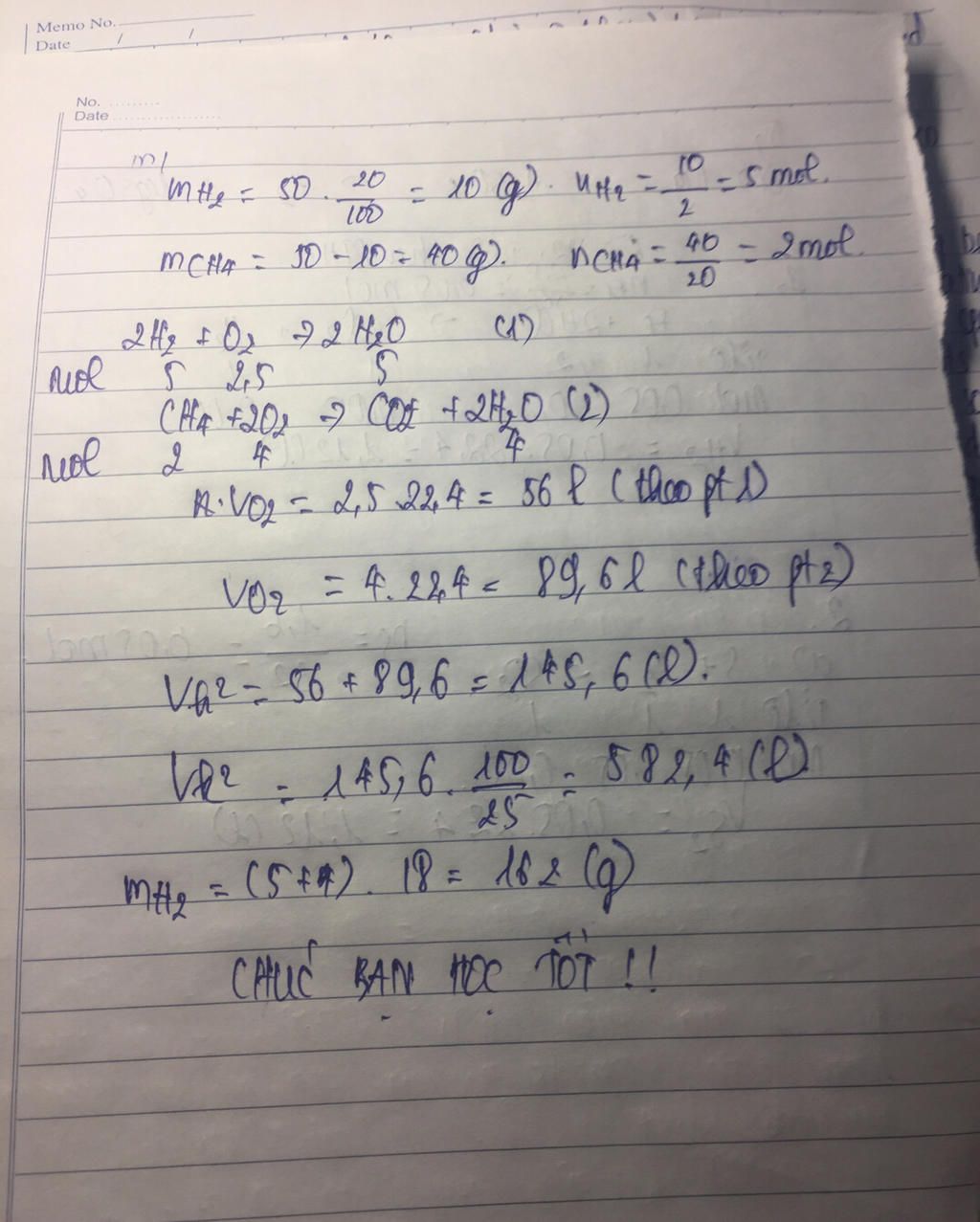Bài 9: Đốt cháy hoàn toàn 50 g hhX (gồm H2 và CH4) trong đó H2 chiếm 20% về khối lượng. a. Tính thể tích không khí cần dùng biết rằng khí oxi chiếm 25% thể tích không khí. b. Đã tạo ra bao nhiêu gam nước?
2 câu trả lời
Đáp án:
Giải thích các bước giải:
`CH_4 + 2O_2` $\xrightarrow{t°}$ `CO_2 + 2H_2O`
`2H_2 + O_2`$\xrightarrow[]{t°}$ `2H_2O`
`m_{H_2} = {20 . 50}/{100} = 10g`
`n_{H_2} = {10}/2 = 5 mol`
`n_{O_2} = 1/2 n_{H_2} = 2,5 mol`
`m_{CH_4} = 50 - 10 = 40g`
`n_{CH_4} = {40}/{16} = 2,5 mol`
`n_{O_2} = 2n_{CH_4} = 5 mol`
`n_{O_2} = 2,5 + 5 = 7,5 mol`
`V_{kk} = {7,5.22,4.100}/{25} = 672l`
b) `n_{H_2O} = 2n_{CH_4} + n_{H_2}`
`= 5 + 5 = 10 mol`
`m_{H_2O} = 10 . 18 = 180g`
Chúc bạn học tốt #aura