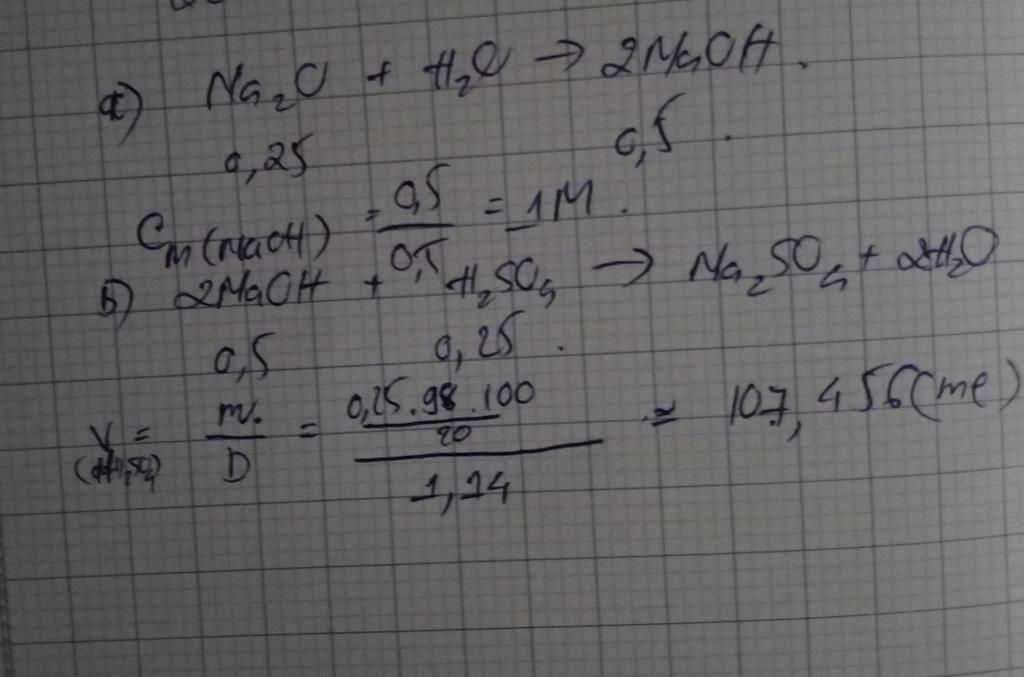Bài 6: Cho 15,5g Natri oxit tác dụng với nước, thu được 500 ml dung dịch bazơ. a) Việt phương trình hóa học và tính nông độ mol của dung dịch bazơ thu được b) Tính thê tích dung dịch H2SO4 20%, có khối lượng riêng 1,14g/ml cần dùng để trung hòa hết dung dịch bazơ nói trên Nhớ có tt nữa nhha mn
2 câu trả lời
Bạn tham khảo:
$a/$
$Na_2O+H_2O \to 2NaOH$
$n_{Na_2O}=\dfrac{15,5}{62}=0,25(mol)$
$n_{NaOH}=0,25.2=0,5(mol)$
$CM_{NaOH}=\dfrac{0,5}{0,5}=1M$
$b/$
$2NaOH+H_2SO_4 \to Na_2SO_4+2H_2O$
$n_{H_2SO_4}=\dfrac{0,5}{2}=0,25(mol)$
$V_{ddH_2SO_4}=\dfrac{\dfrac{0,25.98.100}{20}}{1,14}=107,46(ml)$