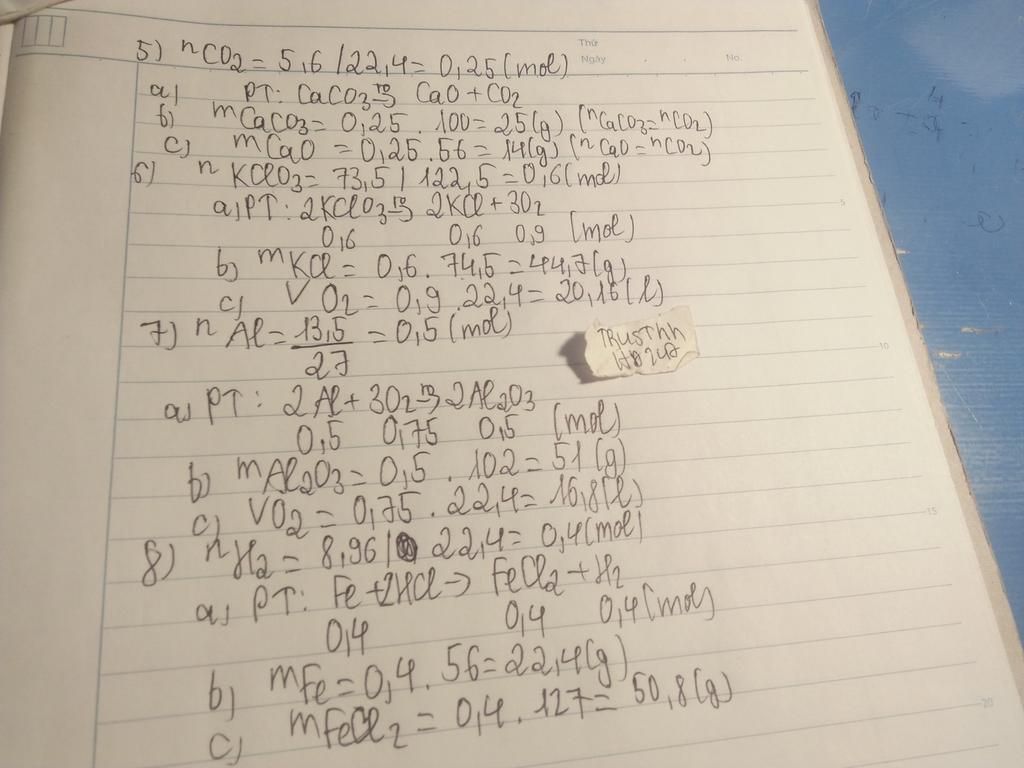Bài 5: Người ta nung canxi cacbonat (CaCO3) ở nhiệt độ cao, thu được canxi oxit (CaO) và 5,6 lít khí cacbonic (CO2). a) Viết PTHH. b) Tính khối lượng CaCO3 tham gia phản ứng. c) Tính khối lượng CaO thu được sau phản ứng. Bài 6:Trong phòng thí nghiệm, để điều chế khí oxi, người ta nung nóng 73,5 g muối KClO3 ở nhiệt độ cao, thu được muối KCl và khí oxi. a) Viết PTHH. b) Tính khối lượng muối KCl. c) Tính thể tích khí oxi sinh ra (đktc). Bài 7:Đốt cháy 13,5 g Al trong bình chứa khí oxi thu được Al2O3. a) Viết PTHH. b) Tính khối lượng Al2O3 thu được sau phản ứng. c) Tính thể tích khí oxi tham gia phản ứng (đktc). Bài 8: Cho cây đinh sắt vào dung dịch axit clohidric HCl, sau phản ứng thu được muối FeCl2 và 8,96 lít khí hidro (đktc). a) Viết PTHH. b) Tính khối lượng sắt tham gia phản ứng. c) Tính khối lượng muối FeCl2 tạo thành sau phản ứng.
2 câu trả lời
$\text{Đáp án+giải thích các bước giải:}$
$\text{Bài 5:}$
$\text{A.}$
$\text{PTHH: $CaCO_{3}$$\xrightarrow{t^o}$CaO+$CO_{2}$}$
$\text{B.}$
$\text{Ta có: $n_{CO_{2}}$=$\dfrac{5,6}{22,4}$= 0,25 mol}$
$\text{Theo PT ta có: $n_{CaCO_{3}}$=$n_{CO_{2}}$= 0,25 mol}$
$\text{⇒ $m_{CaCO_{3}}$=0,25×100= 25 g}$
$\text{C.}$
$\text{Theo PT ta có: $n_{CaO}$=$n_{CO_{2}}$= 0,25 mol}$
$\text{⇒ $m_{CaO}$=0,25×56= 14 g}$
$\text{Bài 6:}$
$\text{A.}$
$\text{PTHH: $2KClO_{3}$$\xrightarrow{t^o}$2KCl+$3O_{2}$}$
$\text{B.}$
$\text{Ta có: $n_{KClO_{3}}$=$\dfrac{73,5}{122,5}$= 0,6 mol}$
$\text{Theo PT ta có: $n_{KCl}$=$n_{KClO_{3}}$= 0,6 mol}$
$\text{⇒ $m_{KCl}$=0,6×74,5= 44,7 g}$
$\text{C.}$
$\text{Theo PT ta có: $n_{O_{2}}$=$\dfrac{3}{2}$×0,6= 0,9 mol}$
$\text{⇒ $V_{O_{2}}$=0,9×22,4= 20,16 lít}$
$\text{Bài 7:}$
$\text{A.}$
$\text{PTHH: 4Al+$3O_{2}$$\xrightarrow{t^o}$$2Al_{2}O_{3}$}$
$\text{B.}$
$\text{Ta có: $n_{Al}$=$\dfrac{13,5}{27}$= 0,5 mol}$
$\text{Theo PT ta có: $n_{Al_{2}O_{3}}$=$\dfrac{2}{4}$×0,5= 0,25 mol}$
$\text{⇒ $m_{Al_{2}O_{3}}$=0,25×102= 25,5 g}$
$\text{C.}$
$\text{Theo PT ta có: $n_{O_{2}}$=$\dfrac{3}{4}$×0,5= 0,375 mol}$
$\text{⇒ $V_{O_{2}}$=0,375×22,4= 8,4 lít}$
$\text{Bài 8:}$
$\text{A.}$
$\text{PTHH: Fe+2HCl→$FeCl_{2}$+$H_{2}$}$
$\text{B.}$
$\text{Ta có: $n_{H_{2}}$=$\dfrac{8,96}{22,4}$= 0,4 mol}$
$\text{Theo PT ta có: $n_{Fe}$=$n_{H_{2}}$= 0,4 mol}$
$\text{⇒ $m_{Fe}$=0,4×56= 22,4 g}$
$\text{C.}$
$\text{Theo PT ta có: $n_{FeCl_{2}}$=$n_{H_{2}}$= 0,4 mol}$
$\text{⇒ $m_{FeCl_{2}}$=0,4×127= 50,8 g}$