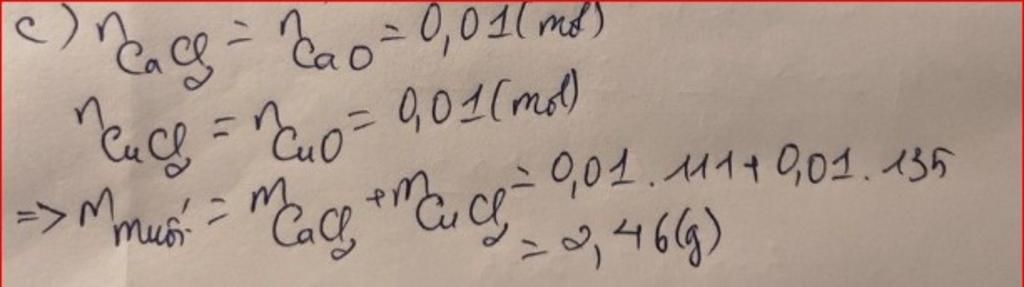1. Cho 14,4g hỗn hợp X gồm Cụ và CuO tác dụng vừa đủ với 500ml dung dịch HCl 0,4M. Vậy khối lượng của đồng trong hỗn hợp trên là? 2. Hòa tan hoàn toàn 1,36 gam hỗn hợp CaO và CuO vào lượng vừa đủ 400ml dung dịch HCl 0,1M a, viết các phương trình phản ứng xảy ra? b, Tính thành phần% khối lượng mỗi chất trong hỗn hợp? c, tính khối lượng các muối tạo thành sau phản ứng?
2 câu trả lời
`1)`
`CuO + 2HCl→ CuCl_2+ H_2O`
`n_{HCl}={500}/{1000}. 0,4 = 0,2(mol)`
`n_{CuO}= 1/2n_{HCl}= 0,1(mol)`
`m_{Cu}= 14,4 - 0,1. 80=6,4(g)`
`2)`
`a)`
`CaO+ 2HCl→ CaCl_2+ H_2O`
`CuO+ 2HCl→ CuCl_2+ H_2O`
`b)`
`n_{HCl}={400}/{1000}. 0,1= 0,04(mol)`
`n_{CuO}= x(mol); n_{CaO}= y(mol)`
`m= 80x + 56y = 1,36(1)`
`n_{HCl}= 2(x+ y)= 0,04(2)`
`(1)(2)→ x= y= 0,01(mol)`
`%m_{CuO}={0,01. 80}/{1,36}. 100= 58,82%`
`%m_{CaO}=100-58,82=41,18%`
`c)`
`n_{H_2O}=1/2n_{HCl}= 0,02(mol)`
Bảo toàn khối lượng:
`m_{text{muối}}= 1,36 +0,04. 36,5-0,02. 18=2,46(g)`
Đáp án:
câu 1 :
CuO + HCL -> CuCL2 + H2O
-> nHCL = 0,4 . 0,5 = 0,2 < MOL >
-> nCuO = 0,2 / 2 = 0,1 < MOL >
-> nCu = 14,4 . 0,1 . 80 = 6,4 < gam >
câu 2 :
a > có % mCa41,17 %
%mCuO=58,83%
b) có : mCaCl2=1,11 gam
mCuCl2=1,35 gam
chúng ta gọi : số mol CaO là x
CuO là y.
=> 56x + 80y = 1,36 g
CaO + 2hcl -> cacl2 + h20
cuo + h2cl -> cucl2 + h20
Ta có: nHCl=0,4.0,1=0,04 mol = 2x + 2y
Giải được x=y=0,01
→mCaO=56x=0,56→%mCaO=0,561,36=41,17%→%mCuO=58,83%
Ta có:
nCaCl2=nCuCl2=0,01 mol→mCaCl2=0,01.111=1,11 gam; mCuCl2=0,01.135=1,35 gam
Giải thích các bước giải: