Lý thuyết: Liên kết hydrogen và tương tác van der Waals
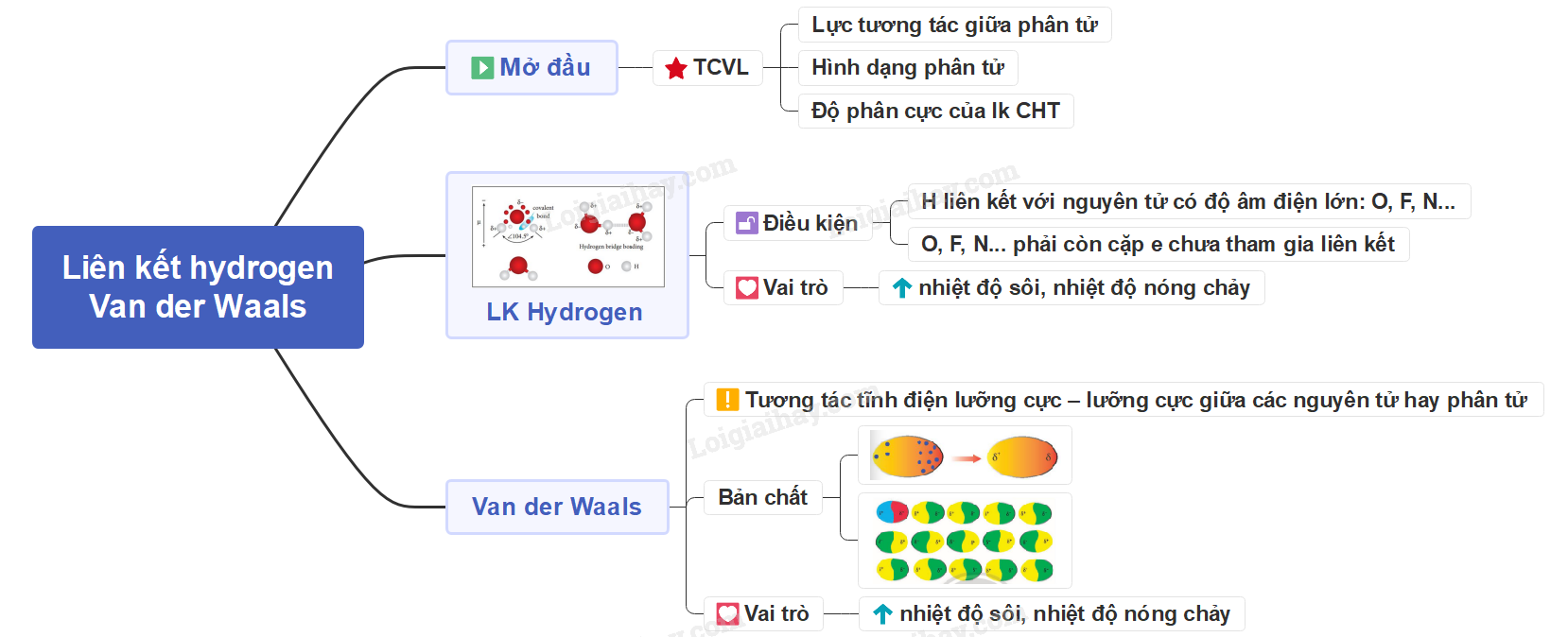
I. Mở đầu
- Các tính chất vật lí của các chất có liên kết cộng hóa trị được quyết định bởi:
+ Lực tương tác giữa các phân tử
+ Hình dạng của phân tử
+ Mức độ phân cực của liên kết cộng hóa trị trong phân tử
- Lực tương tác giữa các phân tử yếu hơn rất nhiều so với lực liên kết ion, liên kết CHT hay liên kết kim loại
- Một số tương tác điển hình giữa các phân tử
+ Liên kết hydrogen
+ Tương tác van der Waals
II. Liên kết hydrogen
1. Bản chất của liên kết hydrogen
- Bản chất: Nguyên tử hydrogen trong phân tử HF, H2O, NH3 rất linh động, có điện tích dương đủ lớn để hút cặp electron hóa trị chưa liên kết trên nguyên tử F, O hoặc N (của phân tử khác) có độ âm điện lớn tạo thành liên kết hydrogen
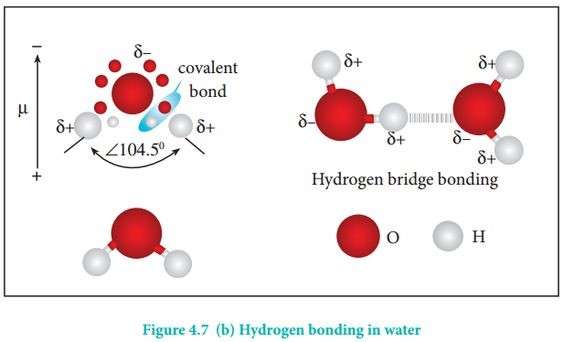
- Điều kiện cần và đủ để tạo thành liên kết hydrogen:
+ Nguyên tử hydrogen liên kết với các nguyên tử có độ âm điện lớn như F, O, N,…
+ Nguyên tử F, O, N,… liên kết với hydrogen phải có ít nhất một cặp electron hóa trị chưa liên kết
- Ví dụ: 1 số kiểu tọa thành liên kết hydrogen
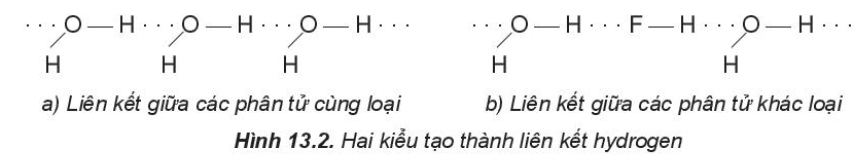
2. Vai trò và ảnh hưởng của liên kết hydrogen tới tính chất vật lí của nước
- Liên kết hydrogen làm tăng nhiệt độ nóng chảy, nhiệt độ sôi của nước
III. Tương tác van der Waals
1. Khái niệm tương tác van der Waals
- Tương tác van der Waals là tương tác tĩnh điện lưỡng cực – lưỡng cực giữa các nguyên tử hay phân tử
- Bản chất:
+ Trong phân tử, các electron không ngừng chuyển động. Khi các electron di chuyển tập trung về một phía bất kì của phân tử sẽ hình thành nên các lưỡng cực tạm thời:
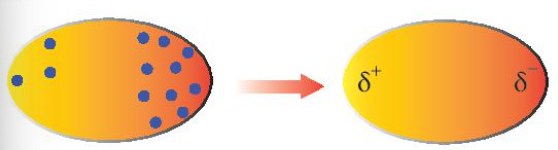
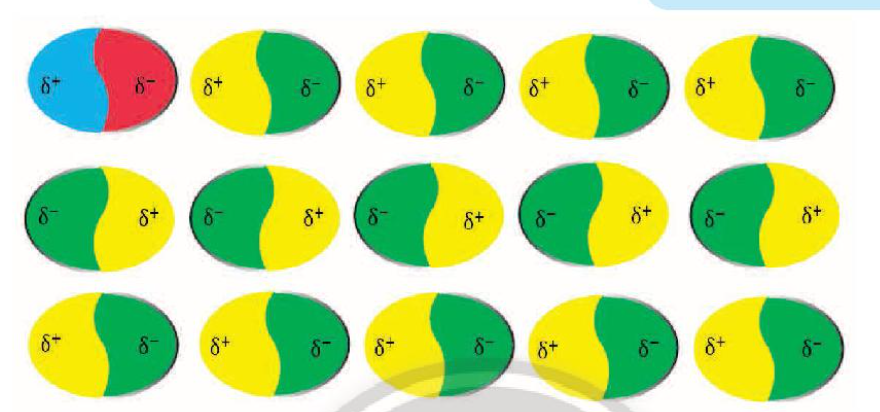
+ Các phân tử có lưỡng cực tạm thời cũng có thể làm các phân tử lân cận xuất hiện các lưỡng cực cảm ứng. Do đó, các phân tử có thể tập hợp thành một mạng lưới với tương tác lưỡng cực cảm ứng, được gọi là tương tác van der Waals
2. Ảnh hưởng của tương tác van der Waals đến nhiệt độ nóng chảy, nhiệt độ sôi của các chất
- Tương tác van der Waals tăng theo sự tăng của số electron trong phân tử. Làm tăng nhiệt độ nóng chảy, nhiệt độ sôi của các chất