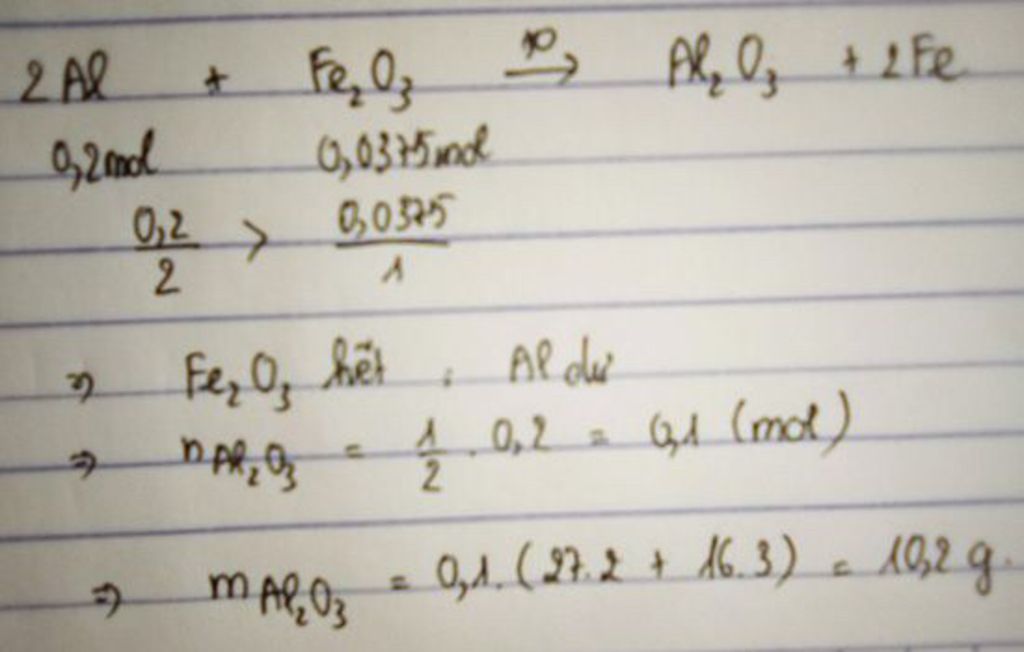Trộn 5,4gam bột Al với 6,0 gam bột Fe2O3 rồi đun nóng để thực hiện phản ứng nhiệt nhôm. Sau phản ứng ta thu được m gam hỗn hợp rắn. Giá trị của m là?
2 câu trả lời
Đáp án:
Giải thích các bước giải:
$2Al + Fe_2O_3 \xrightarrow{t^o} Al_2O_3 + 2Fe$
`n_{Al}=(5,4)/(27)=0,2(mol)`
`n_{Fe_2O_3}=6/(160)=0,0375(mol)`
Ta có tỷ lệ:
`n_{Al}(=(0,2)/2) > n_{Fe_2O_3}(=(0,0375)/1)`
`=> Al` dư; `Fe_2O_3` hết
Theo pthh:
`n_{Al_2O_3}=n_{Fe_2O_3}=0,0375(mol)`
`n_{Fe}=2.n_{Fe_2O_3}=2.0,0375=0,075(mol)`
`n_{Al dư}=0,2-2.0,0375=0,125(mol)`
`=>m= 102.0,0375 + 56.0,075 + 27.0,125=11,4(g)`
Chúc bạn học tốt~
Câu hỏi trong lớp
Xem thêm