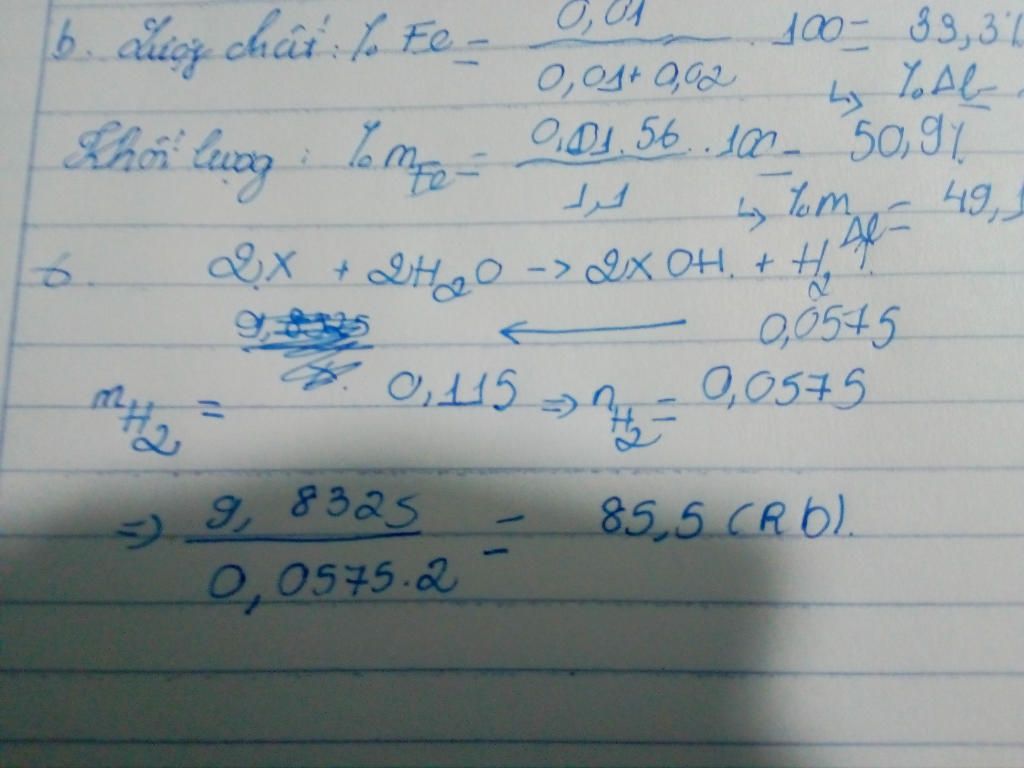Hòa tan hoàn toàn 9,8325 gam một kim loại kiềm vào 50 g nước thu được dung dịch co khoi luonh 59,7175 gam.Kim loại đó là :A.Rb B.Li C.K D.Rb
2 câu trả lời
Đáp án:
Giải thích các bước giải:
có mDD sau phản ứng = m kim loại + mH2O - mH2
⇒ mH2 = 9,8325 + 50 - 59,7175 = 0,115 mol
⇒ nH2 = 0,1152 = 0,0575 mol
Gọi kim loại cần tìm là R
PTHH :
R + H2O → ROH + 12 H2
Theo PT , nR = 2nH2 = 0,0575.2 = 0,115 mol
có mR = 0,115R = 9,8325
⇒ R = 85,5 ( Rb)
Vậy kim loại cần tìm là Rubidi ( đáp án D )
Câu hỏi trong lớp
Xem thêm