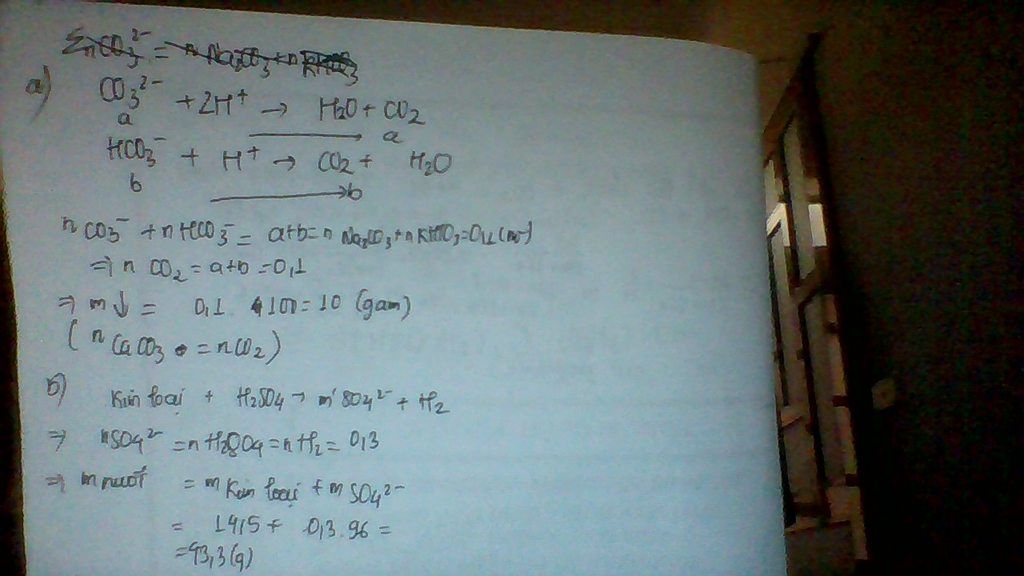Hòa tan hoàn toàn 0,1 mol hh Na2CO3 và KHCO3 vào dd HCl. Dẫn khí thu được vào bình đựng dd Ca(OH)2 dư thì lượng kết tủa tạo ra là m gam. Tính m
2 câu trả lời
Đáp án:
$m_{CaCO_3↓}=10\ g$
Giải thích các bước giải:
PTHH:
\(\begin{array}{l}
CO_3^{2 - } + 2{H^ + } \to {H_2}O + C{O_2} \uparrow \\
HCO_3^ - + {H^ + } \to {H_2}O + C{O_2} \uparrow
\end{array}\)
Nhận thấy $n_{CO_2}=n_{CO_3^{2 - }}+n_{HCO_3^ -}=0,1\ mol$
$CO_2+Ca(OH)_2→CaCO_3↓+H_2O$
$n_{CaCO_3↓}=n_{CO_2}=0,1\ mol$
$→ m_{CaCO_3↓}=0,1.100=10\ g$
Câu hỏi trong lớp
Xem thêm