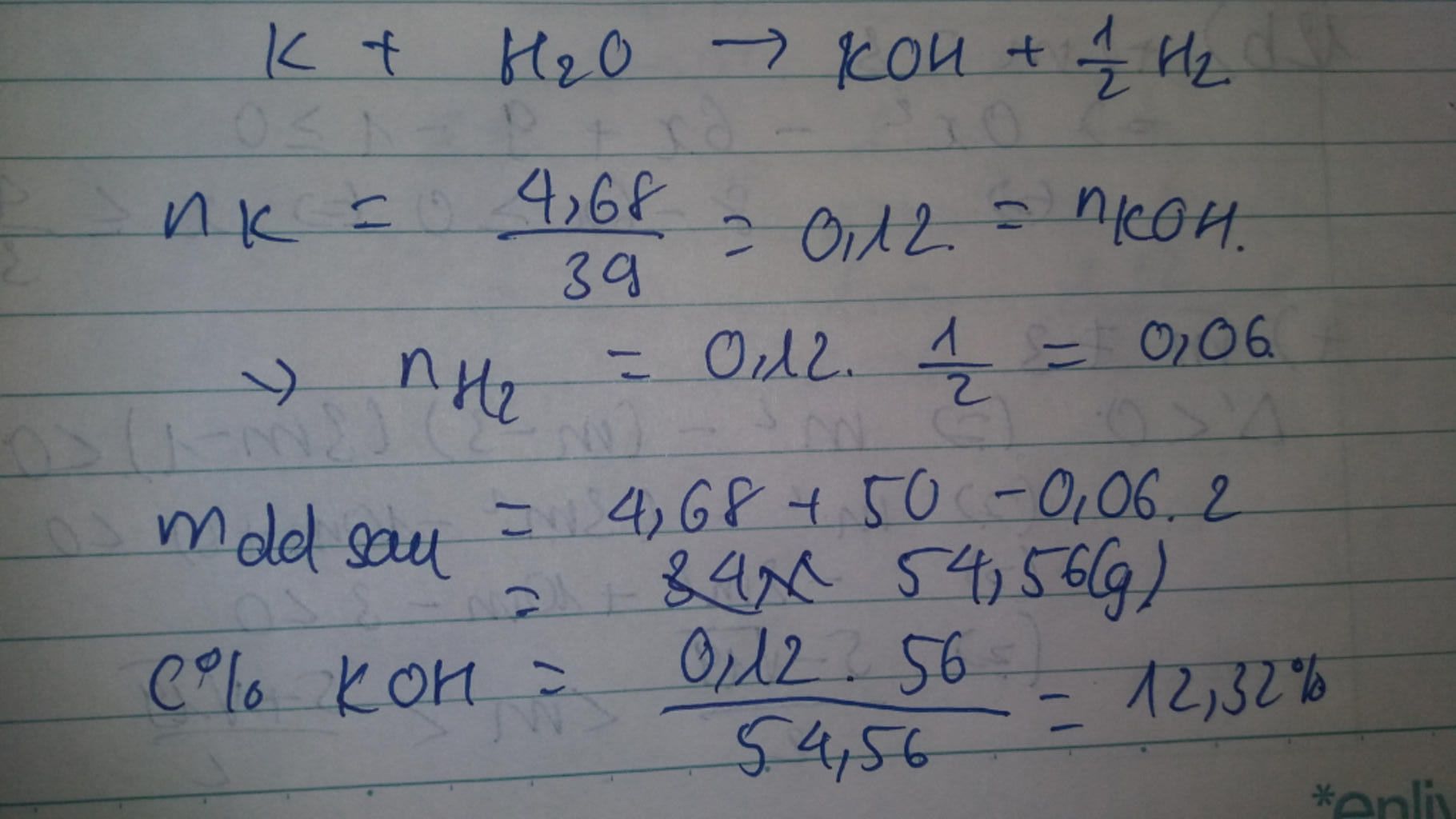Hòa tan 4,68 gam Kali vào 50 g nước nồng độ phần trăm của dung dịch thu được là
2 câu trả lời
Đáp án:
$C\%_{KOH}=12,32\%$
Giải thích các bước giải:
$2K+2H_2O \to 2KOH+H_2$
Ta có: $n_K=\dfrac{4,68}{39}=0,12\ (mol)$
Theo PTHH: $n_{H_2}=\dfrac12 .n_K=0,06\ (mol) \to m_{H_2}=0,12\ (g)$
$m_{\text{dd sau pư}} = m_K + m_{H_2O} - m_{H_2}$
$⇒m_{\text{dd sau pư}} = 4,68+50-0,12=54,56\ (g)$
Mặt khác: $n_{KOH}=n_K=0,12\ (mol) \to m_{KOH}=0,12.56=6,72\ (g)$
$⇒ C\%_{KOH}=\dfrac{6,72}{54,56}.100\%=12,32\%$
Câu hỏi trong lớp
Xem thêm