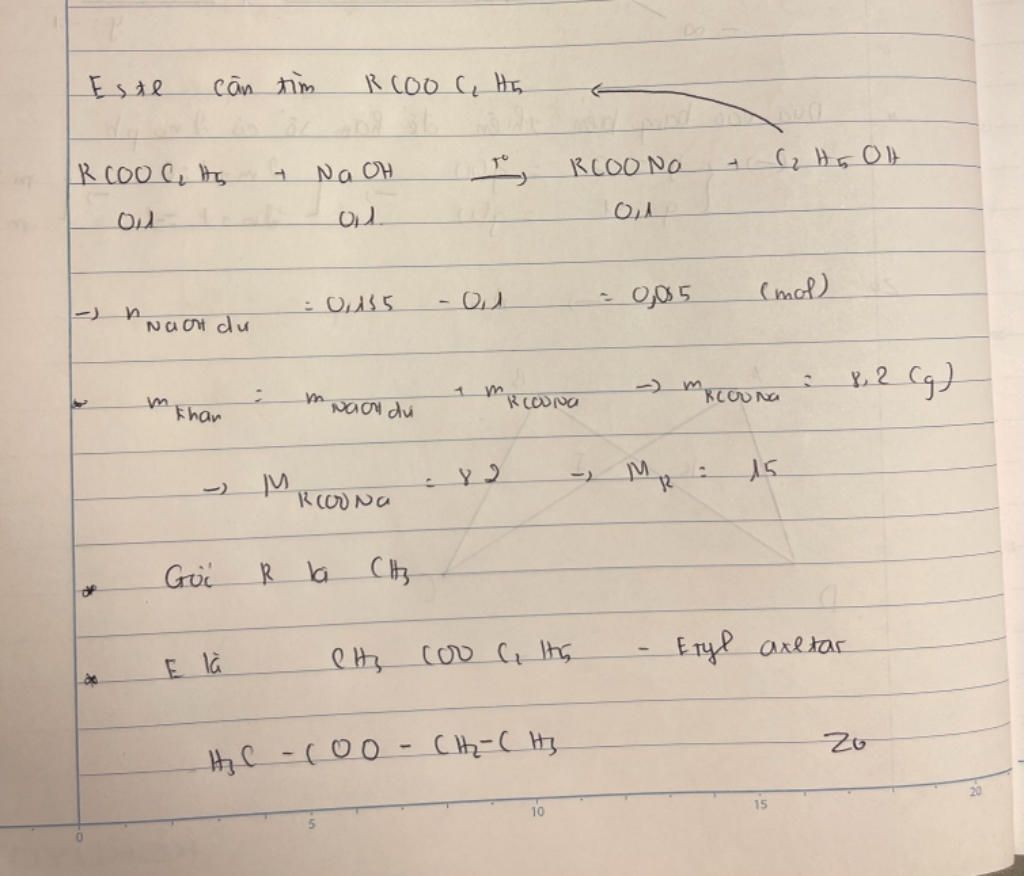giải chi tiết giúp mk đun nóng 0,1 mol este đơn chức X vs 135 ml dd NaOH 1M. Sau khi phản ứng xảy ra hoàn toàn co cạn dd thu dc ancol etylic và 9,6 gam khan tìm CTCT X
2 câu trả lời
Đáp án:
`CH_3COOC_2H_5` ( Etyl axetat )
Giải thích các bước giải:
Gọi công thức hóa học của este đơn chức là `RCOOR'`
- Vì sau phản ứng thu được `:C_2H_5OH`
` \to R'` là `C_2H_5`
` \to` Công thức hóa học của este là `RCOOC_2H_5`
`n_{NaOH}=1.0,135=0,135(mol)`
Phương trình hóa học :
`RCOOC_2H_5+NaOH \to RCOONa+C_2H_5OH`
Xét tỉ lệ , ta thấy `:\frac{0,1}{1} < \frac{0,135}{1}`
` \to NaOH` dư , tính theo este
Theo phương trình hóa học :
$n_{NaOH(pứ)}=n_{RCOONa}=n_{este}=0,1(mol)$
` \to n_{NaOH(dư)}=0,135-0,1=0,035(mol)`
Mặt khác $:m_{chất.rắn}=m_{NaOH(dư)}+m_{RCOONa}$
Hay `:9,6=0,035.40+m_{RCOONa}`
` \to m_{RCOONa}=9,6-0,035.40=8,2(g)`
` \to M_{RCOONa}=\frac{8,2}{0,1}=82` $(g/mol)$
` \to M_{R}+67=82`
` \to M_{R}=82-67=15=M_{CH_3}`
Suy ra `R` là `:CH_3`
` \to` Công thức phân tủa ủa `X` là `:CH_3COOC_2H_5` ( Etyl axetat )