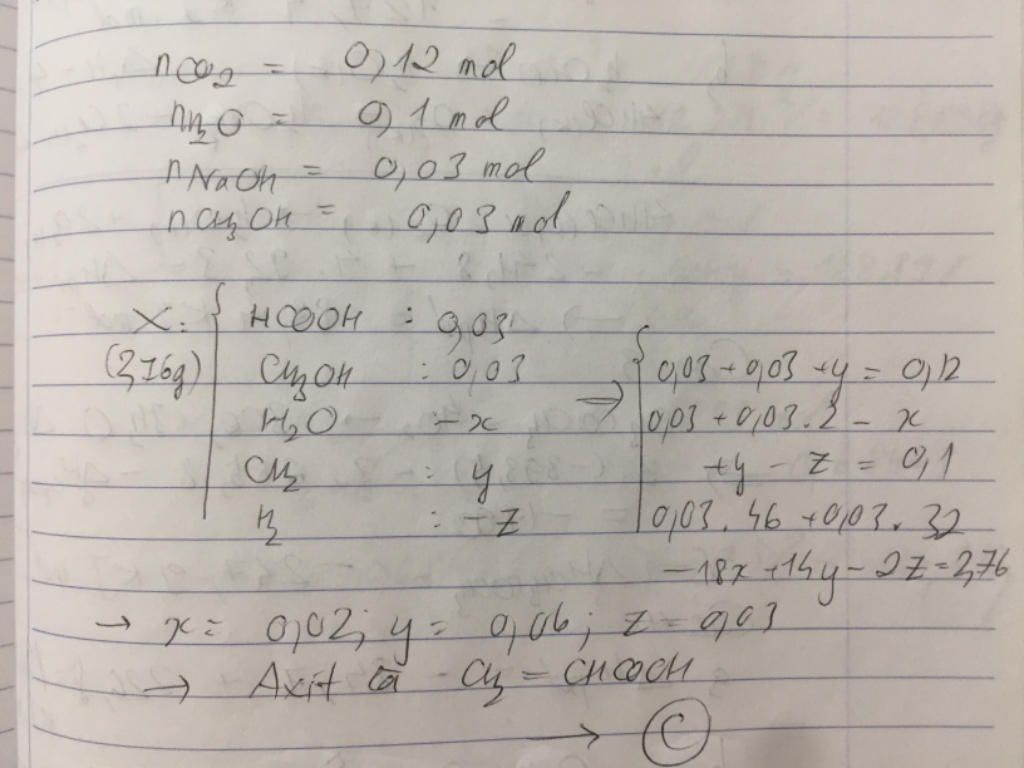Đốt cháy hoàn toàn 2,76 gam hỗn hợp X gồm CxHyCOOH, CxHyCOOCH3, CH3OH thu được 2,688 lít CO2 (đktc) và 1,8 gam H2O. Mặt khác, cho 2,76 gam X phản ứng vừa đủ với 30 ml dung dịch NaOH 1M, thu được 0,96 gam CH3OH. Công thức của CxHyCOOH là A. C2H5COOH B.CH3COOH C. C2H3COOH D. C3H5COOH
2 câu trả lời
Ta xét phản ứng của X với NaOH:
CxHyCOOH + NaOH --> CxHyCOONa + H2O
CxHyCOOCH3 + NaOH --> CxHyCOONa + CH3OH
Có: nNaOH = nCxHyCOOH + nCxHyCOOCH3 = 1*0,03= 0,03(mol);
nCH3OH + nCxHyCOOCH3 = 0,96/32 = 0,03 (mol)
Nhận thấy, 2 đại lượng ta vừa tính được ở trên bằng nhau nên:
Ta quy đổi hỗn hợp X thành CxHyCOOCH3 và H2O. Xét phản ứng đốt cháy X:
CxHyCOOCH3 + (x + y/4 + 0,75)O2 -t0-> (x+2)CO2 + (y/2+1,5)H2O
Có: nCO2 = 2,688/22,4 = 0,12(mol); nH2O = 1,8/18 = 0,1(mol)
Bảo toàn khối lượng => nO(nguyên tử trong X) = (2,76-0,12*12-0,1*2)/16 = 0,07
=> 2nCxHyCOOCH3 + nH2O = 0,07(mol). Mà theo dữ kiện trên: nNaOH = 0,03(mol)
=> nCxHyCOOCH3 = 0,03(mol) => nH2O = 0,07 - 0,03*2 = 0,01 (mol)
=> x = 0,12/0,03 - 2 = 2; y = (0,1-0,01)*2/0,03 - 3 = 3
=> CxHyCOOH là C2H3COOH => chọn C