Dẫn 3,36 lít(đktc) CO2 vào 400 ml dung dich chứ đồng thời KOH 0,1M và Ba(OH)2 0,15M đến khi phản ứng xảy ra hoàn toàn a)Nêu hiện tượng , viết các phương trình hoá học của các phản ứng xảy ra và tính khối lượng kết tủa tạo thành b) Vẽ đồ thị biểu diễn sự phụ thuộc của số mol kết tủa theo số mol CO2
2 câu trả lời
Đáp án:
Giải thích các bước giải:
$n_{CO_2} = 0,15 (mol)$
$n_{Ba(OH)_2} = 0,15.0,4 = 0,06 (mol)$
$n_{KOH} = 0,04 (mol)$
a, Hiện tượng:
- Khi sục khí $CO_2$ lập tức có kết tủa trắng đến mức cực đại thì dừng và khi sục hết có một phần kết tủa bị hòa tan
Thứ tự phản ứng như sau
$Ba(OH)_2 + CO_2 → BaCO_3 + H_2O$
$KOH + CO_2 → K_2CO_3 + H_2O$
$K_2CO_3 + CO_2 + H_2O → 2KHCO_3$
$BaCO_3 + CO_2 + H_2O → Ba(HCO_3)_2$
$n_{BaCO_3} = 0,06 - ( 0,15 - 0,06 - 0,04 ) = 0,01 (mol)$
$m_{BaCO_3} = 0,01 . 197 = 1,97 (g)$
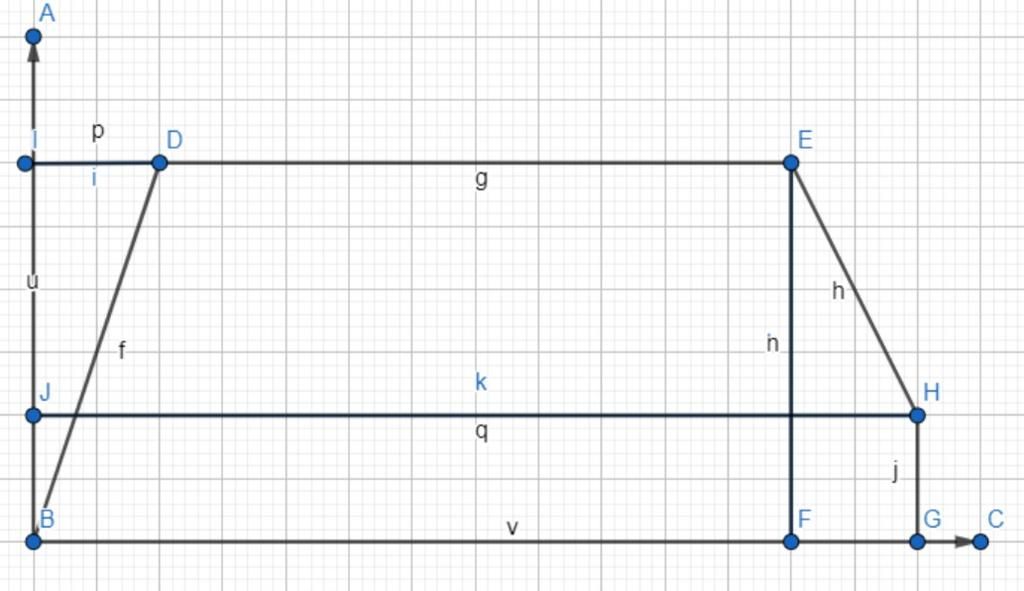
b,
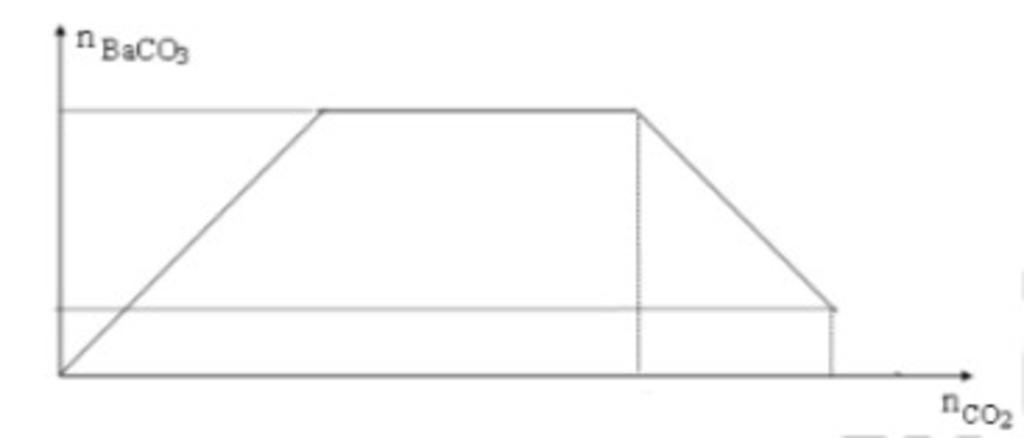
`BA` là `nBaCO3`
`BC` là `nCO2`
các `PTHH` có thể xẩy ra :
`Ba(OH)2+CO2→BaCO3+H2O(1)`
`KOH+CO2→K2CO3+H2O(2)`
`K2CO3+H2O+CO2→2KHCO3(3)`
`BaCO3+H2O+CO2→2Ba(HCO3)2(4)`
hiện tương :
`+)`có kết tủa trắng
`+)` một phần kết tủa bị hòa tan
`th1: Bazow` dư
`nCO2=nBaCO3=(3,36)/(22,4)=0,15`
`=>m↓=0,15.197=29,55`
`=>` loại
vậy `Bazow` hết
`nBaCO3=0,4.0,15-(0,15-0,4.0,15-0,4.0,1)=0,01`
`⇒mBaCO3=0,01.197=1,97g`