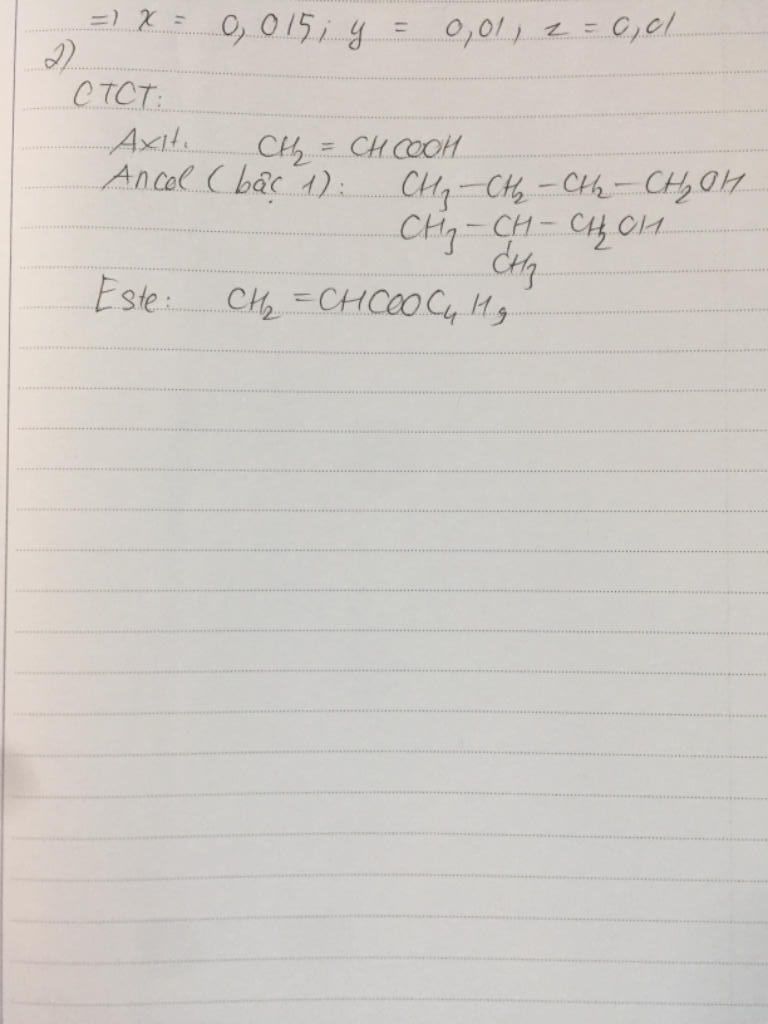Có một hỗn hợp A gồm x mol axit cacboxylic đơn chức, y mol rượu đơn chức và z mol este tạo bởi axit với rượu đó. Khối lượng hỗn hợp là 3,1 gam. Lấy 1,55 gam hỗn hợp A đem đốt cháy hoàn toàn, thu được 1,736 lít khí CO 2 (đktc) và 1,26 gam nước. Lấy 1,55 gam hỗn hợp A cho phản ứng vừa hết với 125 ml dung dịch NaOH 0,1M, sau phản ứng trong hỗn hợp tạo ra có p gam muối và 0,74 gam rượu. Tách lấy toàn bộ lượng rượu rồi cho tác dụng với CuO dư, đốt nóng, tiếp theo cho anđehít tạo ra tác dụng hết với AgNO 3 dư trong dung dịch amoniăc tạo ra 2,16 gam bạc kim loại. 1) Viết các phương trình phản ứng, tính x, y, z, p. 2) Xác định công thức cấu tạo các chất có trong hỗn hợp A. 3) Tính thành phần % theo khối lượng của các chất trong A. Mọi người giúp mình nhanh với ạ >.<
2 câu trả lời
Đáp án:
1. $x = 0,0075;\,\,y = 0,005;\,\,z = 0,005$
2.
Axit là \(CH_2=CH-COOH\)
Ancol là \(CH_3-CH_2-CH_2-CH_2-OH\)
Este là \(CH_2=CH-COOCH_2-CH_2-CH_2-CH_3\)
3.
$ \% {m_{axit}} = 34,84\% ;\\\% {m_{ancol}} = 23,87\% \\ \% {m_{este}} = 41,29\% $
Giải thích các bước giải:
Vì este tạo bởi axit và rượu đơn chức nên este đơn chức.
Đốt cháy \(A\)
\(A + {O_2}\xrightarrow{{{t^o}}}C{O_2} + {H_2}O\)
Ta có:
\({n_{C{O_2}}} = \dfrac{{1,736}}{{22,4}} = 0,0775{\text{ mol;}}\\{{\text{n}}_{{H_2}O}} = \dfrac{{1,26}}{{18}} = 0,07{\text{ mol}}\)
\( \to {n_C} = 0,0775;{n_H} = 0,14 \to {n_O} = 0,03\)
Cho \(A\) tác dụng với \(NaOH\)
\({n_{NaOH}} = 0,125.0,1 = 0,0125{\text{ mol = }}{{\text{n}}_{COO}}\\ \to {n_{OH}} = 0,03 - 0,0125.2 = 0,005mol\)
Ancol tạo ra có dạng \(RCH_2OH\)
\(RC{H_2}OH + CuO\xrightarrow{{{t^o}}}RCHO + Cu + {H_2}O\)
Nếu ancol là \(CH_3OH\) suy ra andehit là \(HCHO\)
Ta có:
\({n_{Ag}} = \dfrac{{2,16}}{{108}} = 0,02 mol \\\to {n_{HCHO}} = 0,005 = {n_{C{H_3}OH}}\\ \to {m_{C{H_3}OH}} = 0,005.32 = 0,16 < 0,74\)
Vậy ancol không phải là \(CH_3OH\)
\( \to {n_{RCHO}} = \frac{1}{2}{n_{Ag}} = {n_{RC{H_2}OH}} = 0,01{\text{ mol}}\)
\( \to {M_{RC{H_2}OH}} = {M_R} + 14 + 17 = \dfrac{{0,74}}{{0,01}} = 74 \\\to {M_R} = 43 \to R:{C_3}{H_7}\)
Vậy ancol là \(C_4H_9OH\)
\( \to {n_{ancol}} = 0,01{\text{ mol}} \to {{\text{n}}_{este}} = z = 0,01 - 0,005 = 0,005{\text{ mol}}\)
\( \to y = 0,01 - 0,005 = 0,005{\text{ mol; x = 0}}{\text{,0125 - 0}}{\text{,005 = 0}}{\text{,0075}}\)
Gọi số \(C\) của axit là \(n\)
Suy ra este có \(n+4\) \(C\)
Bảo toàn \(C\)
\( \to 0,0075.n + 0,005.4 + 0,005.(n + 4) = 0,0775 \to n = 3\)
Ta có:
\({n_{C{O_2}}} - {n_{{H_2}O}} = 0,0775 - 0,07 = 0,0075 = {n_{axit}} + {n_{este}} - {n_{ancol}}\)
Vậy axit chứa 1 \(\pi\)
Suy ra axit là \(CH_2=CH-COOH\)
Ancol là \(CH_3-CH_2-CH_2-CH_2-OH\)
Este là \(CH_2=CH-COOCH_2-CH_2-CH_2-CH_3\)
Phản ứng xảy ra:
\(C{H_2} = CHCOOH + 3{O_2}\xrightarrow{{{t^o}}}3C{O_2} + 2{H_2}O\)
\({C_4}{H_9}OH + 6{O_2}\xrightarrow{{{t^o}}}4C{O_2} + 5{H_2}O\)
\(C{H_2} = CHCOO{C_4}{H_9} + 9{O_2}\xrightarrow{{{t^o}}}7C{O_2} + 6{H_2}O\)
\(C{H_2} = CHCOOH + NaOH\xrightarrow{{}}C{H_2} = CHCOONa + {H_2}O\)
\(C{H_2} = CHCOO{C_4}{H_9} + NaOH\xrightarrow{{}}C{H_2} = CHCOONa + {C_4}{H_9}OH\)
\({C_4}{H_9}OH + CuO\xrightarrow{{{t^o}}}{C_3}{H_7}CHO + Cu + {H_2}O\)
Ta có:
\({m_{axit}} = 0,0075.72 = 0,54{\text{ gam;}}\\{{\text{m}}_{ancol}} = 0,005.74 = 0,37{\text{ gam}}\) \( \to \% {m_{axit}} = \dfrac{{0,54}}{{1,55}} = 34,84\% ;\\\% {m_{ancol}} = \dfrac{{0,37}}{{1,55}} = 23,87\% \\\to \% {m_{este}} = 41,29\% \)