Cho 3,07 gam hỗn hợp bột kim loại X gồm Al và Fe vào 150 ml dung dịch hỗn hợp gồmFe(NO3)3 1,0 M và AgNO3 0,5 M, khuấy đều, sau phản ứng thu được m gam kim loại và dung dịch Y (chứaba muối). Cho từ từ dung dịch NaOH dư, lấy kết tủa nung đến khối lượng không đổi được 16,0 gam chất rắnkhan. Biết các phản ứng xảy ra hoàn toàn.a. Viết phương trình phản ứng có thể đã xảy ra.b. Tính m và phần trăm khối lượng của Al và Fe trong X
2 câu trả lời
Đáp án:
Giải thích các bước giải:
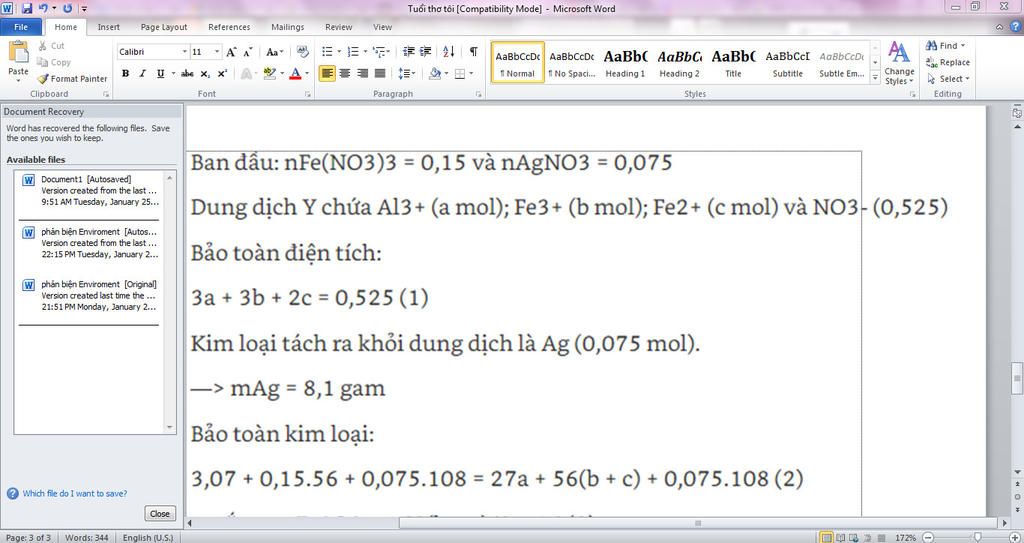
ban đầu : nFE (NO3) 3=0,15 Và nAgNO3 =0,075
dung dịch Y chiếm AL3 + (a mol ) và NO3 - (0,525)
bảo toàn diện tích
3a+3b + 2c = 0,525 (1)
kim loại tách ra ở dung dịch là Ag (0,075mol)
⇒mAg =8,1gam
bảo toàn kim loại
3,07 + 0,15.56+0,075.108=27a+ 56 (b+c)+0,075 .108(2)
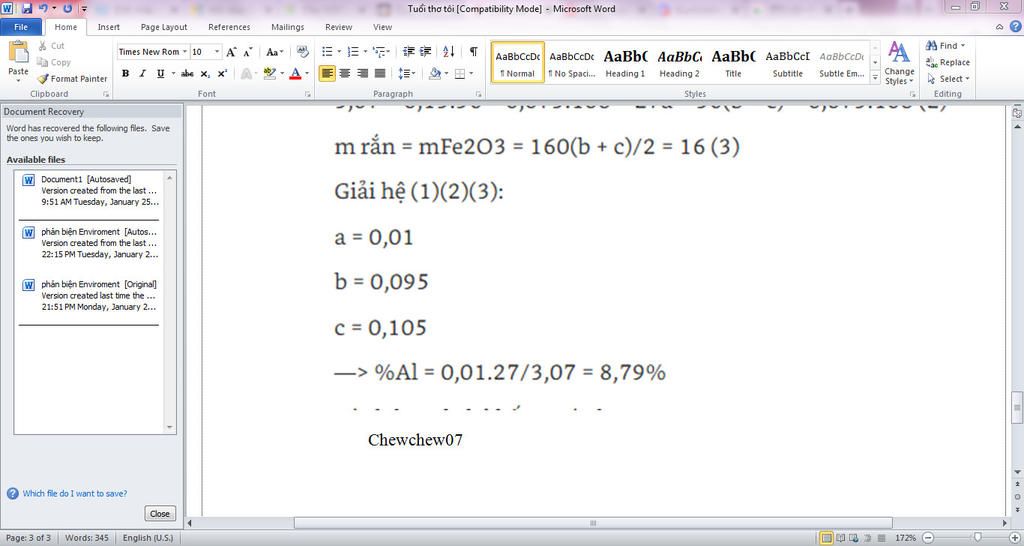
m rắn = mFE2O3 = 160 (b+c) /2=16(3)
giải hệ (1)(2)(3)
A=0,01
B=0,095
C=0,105
⇒ % Al =0,01 .27/3,07=8,79%
@quochuy
Câu hỏi trong lớp
Xem thêm