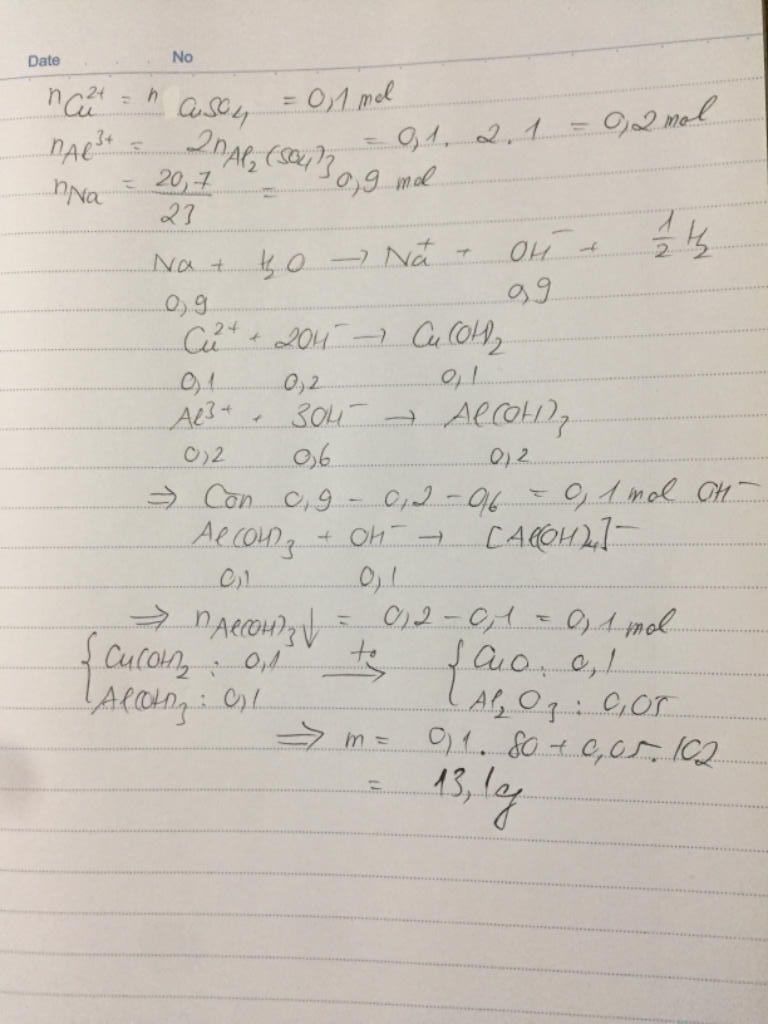cho 100ml đ hỗn hợp CuSO4 1M và Al2(SO4)3 1M tác dụng với 20,7g Na lọc kết tủa nung đến k đổi tìm m chất rắn
2 câu trả lời
$n_{CuSO_4}=0,1(mol)$
$n_{Al_2(SO_4)_3}=0,1(mol)$
$n_{Na}=0,9(mol)$
$2Na+2H_2O→2NaOH+H_2$
$2NaOH+CuSO_4→Na_2SO_4+Cu(OH)_2↓$
0,2 0,1 0,1
$6NaOH+Al_2(SO_4)_3→3Na_2SO_4+2Al(OH)_3$
0,6 0,1 0,2
$2NaOH+2Al(OH)_3→2NaAlO_2+4H_2O$
0,1 0,1
$Cu(OH)_2\xrightarrow{{t^o}}CuO+H_2O$
$2Al(OH)_3\xrightarrow{{t^o}}Al_2O_3+3H_2O$
Theo phương trình, ta có:
$∑n_{NaOH p/ư}=0,1.2+0.1.6+0.1.2=1(mol)$
Vì $1<0,9$⇒Thiếu $NaOH$ để phản ứng hết hoàn toàn với hỗn hợp
⇒Dư $0,1$ mol $Al(OH)_3$
⇒$m=0,1.80+0,05.102=13,1(g)$
Câu hỏi trong lớp
Xem thêm