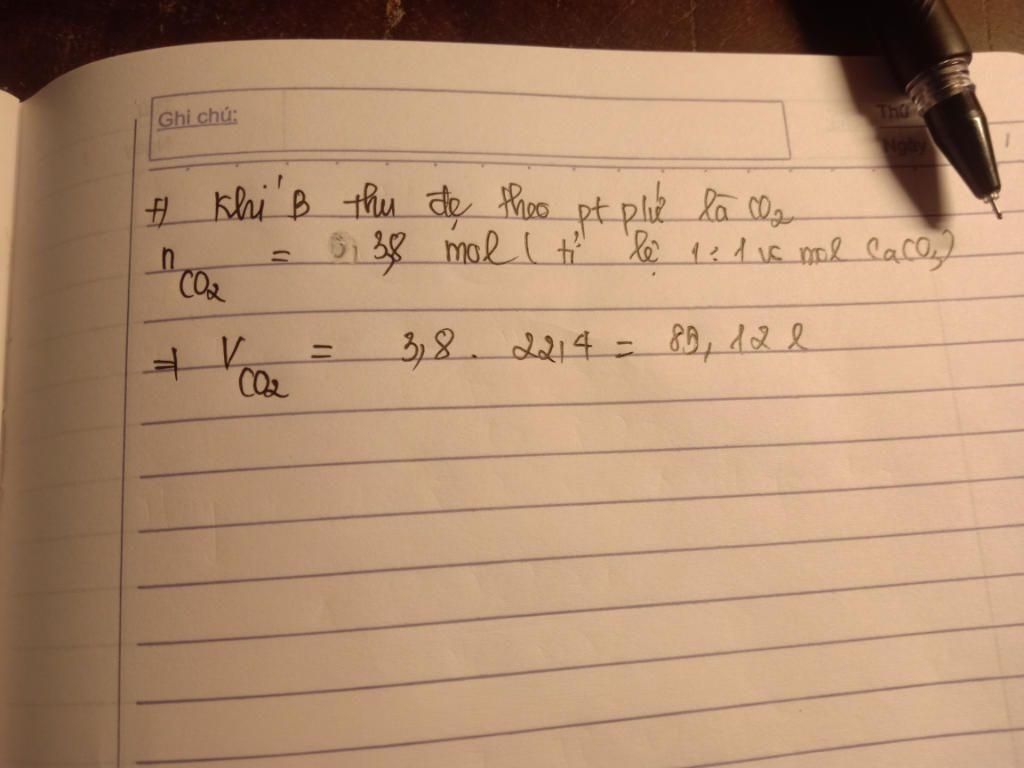Câu 4. (2,5 điểm) Nung 500gam đá vôi chứa 95% CaCO3 phần còn lại là tạp chất không bị phân huỷ. Sau một thời gian người ta thu được chất rắn A và khí B. 1) Viết phương trình hóa học xảy ra và tính khối lượng chất rắn A thu được, biết hiệu suất phân huỷ CaCO3 là 80% 2) Tính % khối lượng CaO có trong chất rắn A và thể tích khí B thu được (ở đktc). Câu 5. (2,0 điểm) 1) Có 16ml dung dịch HCl nồng độ a mol/l (gọi dung dịch A). Thêm nước cất vào dung dịch A cho đến khi thể tích dung dịch là 200ml, lúc này nồng độ của dung dịch là 0,1. Tính a? 2) Lấy 10ml dung dịch A trung hòa vừa đủ V lít dung dịch NaOH 0,5M. Tính thể tích và CM của dung dịch sau phản ứng. Câu 6. (3,5 điểm) Hỗn hợp A gồm NxO, SO2, CO2 trong đó NxO chiếm 30%, SO2 chiếm 30% về thể tích, còn lại của CO2. Trong hỗn hợp NxO chiếm 19,651% về khối lượng. Xác định công thức hóa học của NxO và tính tỉ khối của A so với H2 Câu 7. (3,5 điểm) Cho 19,5 gam Zn tác dụng với dung dịch loãng có chứa 39,2 gam axit sunfuric. a) Tính thể tích khí H2 thu được ở điều kiện tiêu chuẩn. b) Dẫn toàn bộ lượng khí thu được ở trên qua hỗn hợp A gồm CuO và Fe3O4 nung nóng thì thấy khối lượng hỗn hợp A giảm m gam. Xác định giá trị của m.
2 câu trả lời
Câu 4 :-klg CaCO3 trong đá vôi là :
$m_CaCO3$=500×95%=475(g)
-số mol CaCO3 là : $n_CaCO3$=$\dfrac{475}{100}$=4,75(mol)
1)-PTHH xảy ra: CaCO3 → CaO+ CO2 (thêm nhiệt độ ở điều kiện nhé)
4,75mol 4,75mol
-klg CaO thu được là : $m_CaO%=4,75×56×80%=212,8 (g)
-do H%=80% nên dư 20% CaCO3
-klg CaCO3 dư là : $mCaCO3_dư$=475×20%=95(g)
-klg chất rắn A là : $m_A$=212,8+95=307,8(g)
2)-% klg CaO trong A là :
$%m_CaO$=$\dfrac{212,8×100%}{307,8}$≈69,14%
Câu hỏi trong lớp
Xem thêm