câu 1:Tính tổng khối lượng theo mg/lít của các ion Ca2+ và Mg2+ có trong một loạ nước tự nhiên. Biết rằng nước này có chứa đồng thời các muối Ca(HCO3)2 Mg(HCO3)2 và CaSO4 với khối lượng tương ứng là 112,5 mg/l, 11,9 mg/l và 54,5 mg/l. câu 2:Có ba cốc đựng lần lượt: nước mưa, nước có tính cứng tạm thời, nước có tính cứng vĩnh cửu. Hãy nhận biết nước đựng trong mỗi cốc bằng phương pháp hóa học. Viết phương trình phản ứng. làm nha: làm hết.
2 câu trả lời
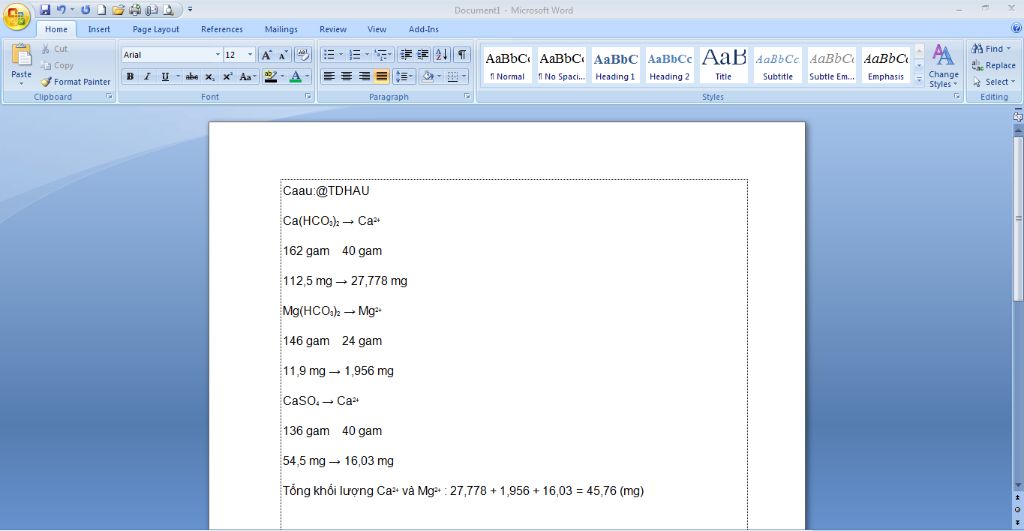
Câu 1:
Xét $1l$ nước tự nhiên.
$m_{Ca(HCO_3)_2}=112,5mg$
$\Rightarrow n_{Ca(HCO_3)_2}=0,7(mmol)$
$m_{CaSO_4}=54,5mg$
$\Rightarrow n_{CaSO_4}=0,4(mmol)$
$\Rightarrow n_{Ca^{2+}}=n_{Ca(HCO_3)_2}+n_{CaSO_4}=1,1(mmol)$
$m_{Ca^{2+}}=40.1,1=44mg$
$\to D_{Ca^{2+}}=44mg/l$
$m_{Mg(HCO_3)_2}=11,9mg$
$\Rightarrow n_{Mg^{2+}}=n_{Mg(HCO_3)_2}=0,08(mol)$
$m_{Mg^{2+}}=0,08.24=1,92mg$
$\to D_{Mg^{2+}}=1,92mg/l$
Tổng nồng độ $Mg^{2+}$ và $Ca^{2+}$:
$44+1,92=45,92mg/l$
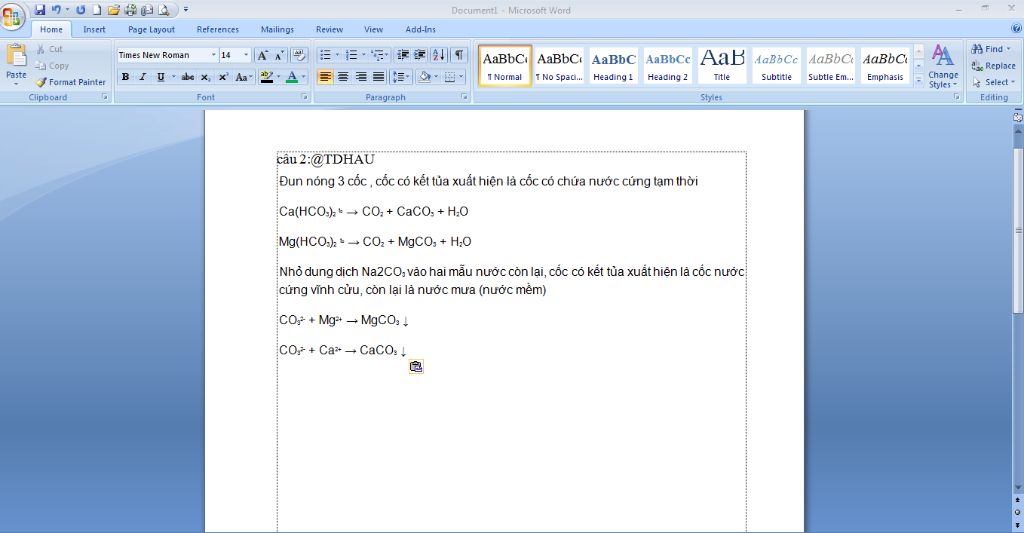
Câu 2:
Đun nóng 3 mẫu nước. Nước cứng tạm thời có kết tủa xuất hiện.
$R(HCO_3)_2\buildrel{{t^o}}\over\to RCO_3\downarrow+CO_2+H_2O$
$(R: Mg, Ca)$
Nhỏ dd $BaCl_2$ vào 2 mẫu nước còn lại. Nước cứng vĩnh cửu có kết tủa trắng. Còn lại nước mưa.
$RSO_4+BaCl_2\to BaSO_4\downarrow+RCl_2$
$(R: Mg, Ca)$
Câu hỏi trong lớp
Xem thêm