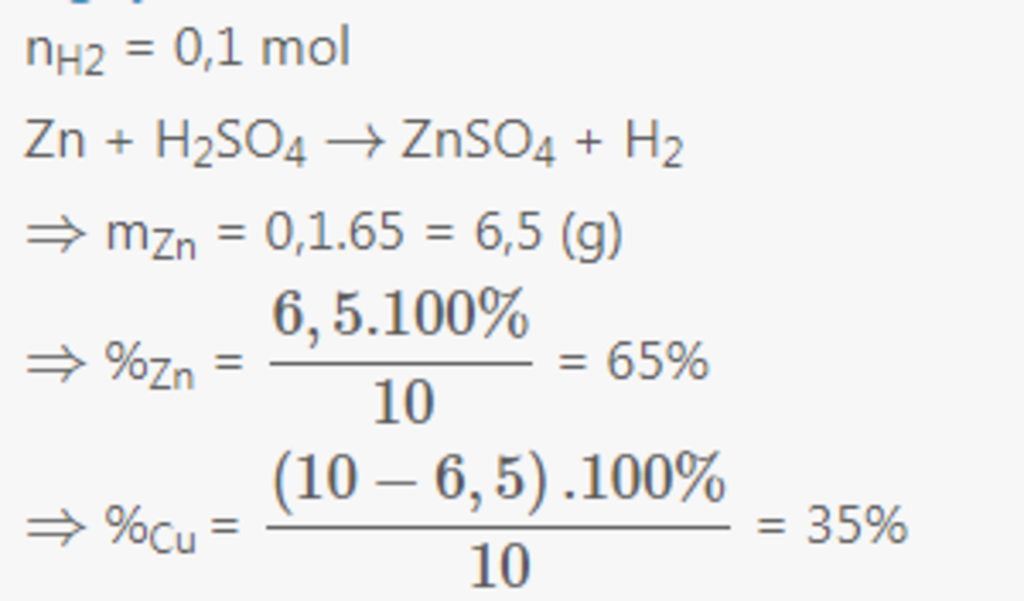Bài 1: Cho 10g hỗn hợp gồm kẽm và đồng tác dụng với axit sunfuric loãng thì thu được 2,24 lít hiđro (đktc). Tính thành phần phần trăm về khối lượng trong hỗn hợp trên. Bài 2: Hòa tan 5,2 g hỗn hợp gồm Magie và sắt bằng dung dịch axit clohiđric 1M thì thu được 3,36 lít hiđro (đktc). a) Tính phần trăm theo khối lượng mỗi kim loại b) Tính thể tích dung dịch axit clohiđric đã dùng
2 câu trả lời
Đáp án:
Bài 1: %mZn = 65% và %mCu = 35%
Bài 2:
%mMg = 46,15%
%mFe = 53,85%
b)
=> V dd HCl = 0,3 lít
Giải thích các bước giải:
Bài 1: nH2 = 2,24/22,4 = 0,1 mol
Khi cho Zn, Cu vào H2SO4 loãng thì chỉ có Zn phản ứng.
Zn + H2SO4 -> ZnSO4 + H2
0,1 <---------------------------0,1 (mol)
=> mZn = 0,1.65 = 6,5 gam
=> %mZn = (6,5/10).100% = 65%
=> %mCu = 100% - 65% = 35%
Bài 2: nH2 = 3,36/22,4 = 0,15 mol
Đặt nMg = x và nFe = y (mol)
+) m hỗn hợp = 24x + 56y = 5,2 (1)
+) PTHH:
Mg + 2HCl -> MgCl2 + H2
x -----> 2x ----------------> x
Fe + 2HCl -> FeCl2 + H2
y ----> 2y --------------> y
=> nH2 = x + y = 0,15 (2)
Giải hệ (1) và (2) được x = 0,1 và y = 0,05
a)
%mMg = (0,1.24/5,2).100% = 46,15%
%mFe = 100% - 46,15% = 53,85%
b)
nHCl pư = 2x + 2y = 2.0,1 + 2.0,05 = 0,3 mol
=> V dd HCl = n : CM = 0,3 : 1 = 0,3 lít