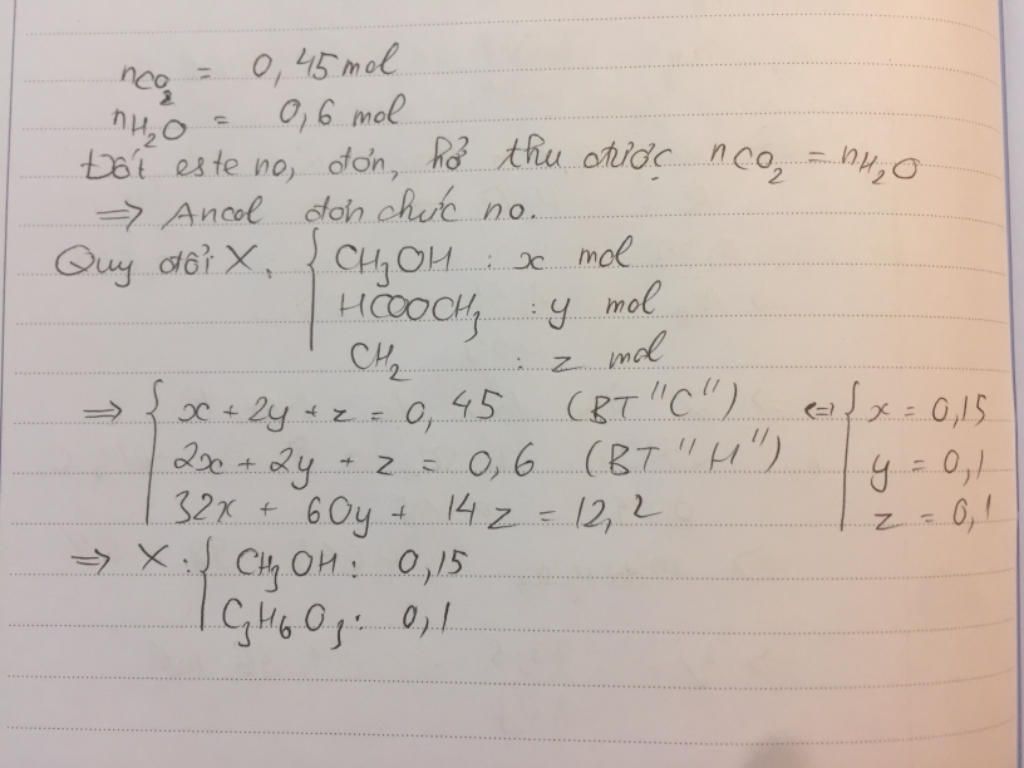60đ!!! Đốt cháy hoàn toàn 12,2 gam hỗn hợp X gồm 1 rượu đơn chức và 1 este no,đơn chức,mạch hở thu được 10,08 lít CO2(đktc) và 10,8 gam H2O.Mặt khác,nếu đun 12,2 gam hỗn hợp X với 120ml dung dịch KOH 1M,sau phản ứng thu được dung dịch Y.Cô cạn dung dịch Y thu được m gam chất rắn khan.Tính m
2 câu trả lời
Đáp án:
Giải thích các bước giải:
$n_{CO_2}=\dfrac{10,08}{22,4}=0,45(mol)<n_{H_2O}=\dfrac{10,8}{18}=0,6(mol)$
⇒X chứa rượu no,đơn chức,mạch hở
Đặt CTTQ của rượu là $C_nH_{2n+1}OH$ và este là $C_mH_{2m}O_2(m≥2)$
$C_nH_{2n+1}OH+\dfrac{3n}{2}O_2→nCO_2+(n+1)H_2O$
na (n+1)a
$C_mH_{2m}O_2+\dfrac{3m-2}{2}O_2→mCO_2+m_{H_2O}$
b mb mb
$⇒a=n_{H_2O}-n_{CO_2}=0,6-0,45=0,15(mol)$
Áp dụng định luật BTKL:
$m_X+m_{O_2}=m_{CO_2}+m_{H_2O}$
$⇒m_{O_2}=m_{CO_2}+m_{H_2O}-m_X=0,45.44+10,8-12,2=18,4(g)$
$⇒n_{O_2}=\dfrac{18,4}{32}=0,575(mol)$
Theo bảo toàn nguyên tố Oxi ta có:
$0,15+2b+2.0,575=2.0,45+0,6⇒b=0,1(mol)$
Số nguyên tử cacbon trung bình:
$\overline{n}=\dfrac{n_{CO_2}}{a+b}=\dfrac{0,45}{0,15+0,1}=1,8⇒n=1(CH_3OH)$
$⇒n_{CO_2}=1.0,15+0,1m=0,45⇒m=3(C_3H_6O_2)$
Xét 2 trường hợp sau:
Trường hợp 1:Este là $HCOOC_2H_5$
$HCOOC_2H_5+KOH→HCOOK+C_2H_5OH$
0,1 0,1 0,1
$⇒n_{KOH còn}=0,12-0,1=0,02(mol)$
$⇒m=m_{HCOOK}+m_{KOH còn}=84.0,1+56.0,02=9,52(g)$
Trường hợp 2: Este là $CH_3COOCH_3$
$CH_3COOCH_3+KOH→CH_3COOK+CH_3OH$
0,1 0,1 0,1
$⇒n_{KOH còn}=0,12-0,1=0,02(mol)$
$⇒m=m_{CH_3COOK}+m_{KOH còn}=98.0,1+56.0,02=10,92(g)$
Đuối quá :v