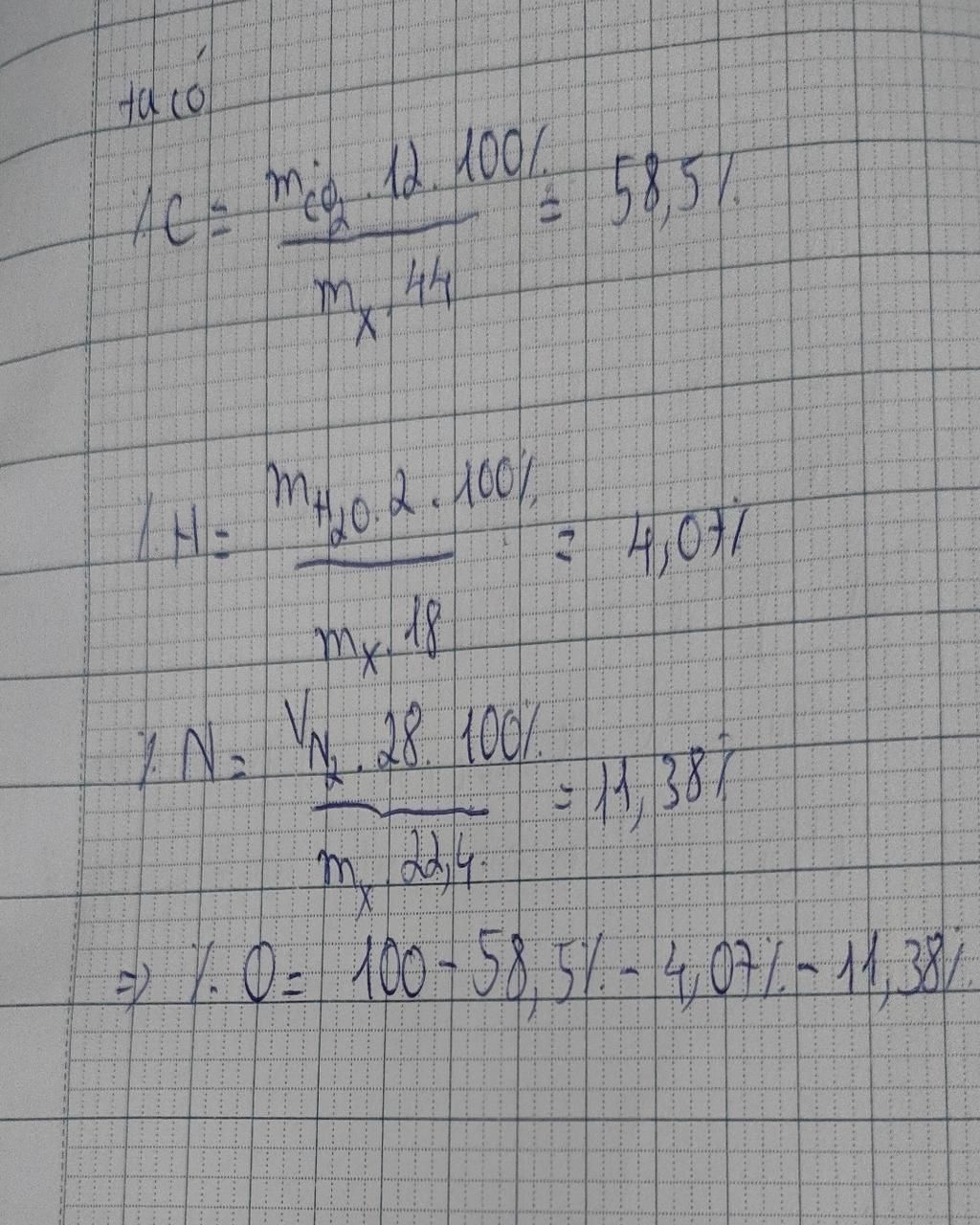(2,0 điểm) Đốt cháy hoàn toàn 1,23g hợp chất hữu cơ X, sau phản ứng thu được 0,45g H2O, 2,64g khí CO2 và 112ml khí N2 (ở đktc). Biết tỉ khối hơi của X so với không khí là 4,242. a/ Xác định thành phần % về khối lượng của mỗi nguyên tố trong hợp chất X. b/ Xác định công thức đơn giản nhất và công thức phân tử của X. Biết nguyên tử khối của các nguyên tố: Ba=137, Cu=64, Fe=56, Ca=40, C=12,
2 câu trả lời
Đáp án:a)
a) `%m_(C)=58,54%`
`%m_(H)=4,07%`
`%m_(O)=26,02%`
`%m_(N)=11,38%`
b) CTĐGN: `C_6H_5O_2N`
CTPT: `C_6H_5O_2N`
Giải thích các bước giải:
`n_(H_2O)=(0,45)/18=0,025mol`
`n_(CO_2)=(2,64)/44=0,06mol`
`n_(N_2)=(0,112)/(22,4)=0,005mol`
Bảo toàn nguyên tố, ta có:
`n_(C)=n_(CO_2)=0,06mol`
`n_(H)=2.n_(H_2O)=0,05mol`
`n_(N)=2.n_(N_2)=0,01mol`
Ta có:
`mC+mH+mN=0,06.12+0,05.1+0,01.14=0,91g`
Vậy trong `A` có chứa nguyên tố `O`
`->m_(O)=1,23-0,91=0,32g`
`%m_(C)=(0,06.12.100)/(1,23)=58,54%`
`%m_(H)=(0,05.1.100)/(1,23)=4,07%`
`%m_(O)=(0,32.100)/(1,23)=26,02%`
`%m_(N)=(0,01.14.100)/(1,23)=11,38%`
b) Ta có:
`nC:nH:nO:nN=0,06:0,05:0,02:0,01=6:5:2:1`
Vậy CTĐGN có dạng `(C_6H_5O_2N)_n`
`M_(X)=4,242.29=123`$g/mol$
`<=>123n=123`
`->n=1`
Vậy CTPT là `C_6H_5O_2N`