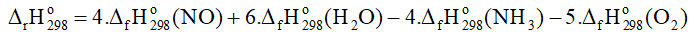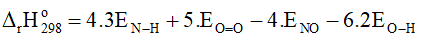Với giải Câu hỏi 8 trang 56 Hóa học lớp 11 Kết nối tri thức chi tiết trong Bài 9: Ôn tập chương 2 giúp học sinh dễ dàng xem và so sánh lời giải từ đó biết cách làm bài tập Hóa học 11. Mời các bạn đón xem:
Giải bài tập Hóa học lớp 11 Bài 9: Ôn tập chương 2
Câu hỏi 8 trang 56 Hóa học 11: Xét phản ứng trong giai đoạn đầu của quá trình Ostwald:
4NH3(g) + 5O2(g)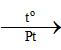
a) Tính 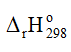
Biết nhiệt tạo thành chuẩn của NH3(g), NO(g) và H2O(g) lần lượt là -45,9 kJ/mol; 90,3 kJ/mol và -241,8 kJ/mol.
b) Tính năng lượng liên kết trong phân tử NO.
Biết năng lượng liên kết N – H, O = O, O – H lần lượt là 386 kJ/mol, 494 kJ/mol và 459 kJ/mol.
Lời giải:
a)
= 4. 90,3 + 6.(-241,8) – 4. (-45,9) = -906 kJ.
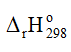
Phản ứng toả nhiệt này cần phải khơi mào, do đó có thể tận dụng nhiệt lượng toả ra này để tiếp diễn phản ứng mà không cần đốt nóng liên tục.
b)
⇒ -906 = 4. 3. 386 + 5.494 – 4. ENO – 6.2. 459
⇒ ENO = 625 kJ/mol.