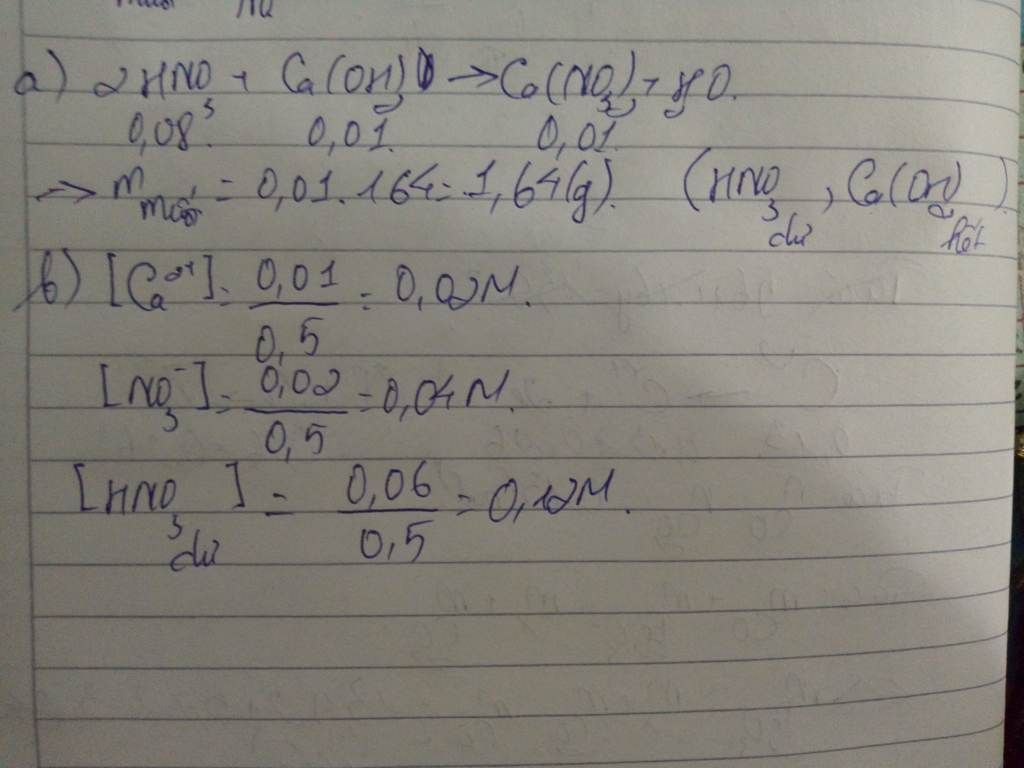trộn 400ml dd HNO3 0,2M với 100ml dd Ca(OH)2 0,1M thu được dd A . a) Tính khối lượng muối thu được, b) tính nồng độ mol/l của các ion trong dd A
2 câu trả lời
Đáp án:viết phương trình tính số mol từng chất ra m muối=0,01.164=1,64g
b)ddA gồm ca(no3)2 và hno3 dư
Ca2+=0,02M
No3-=0,08M
H+=0,04M
Đáp án: a. m=1,64 (g)
b. [Ca 2+]=0,02M
[NO3 -]=0,04M
[HNO3 dư]=0,12M
Giải thích các bước giải:
a. HNO3 dư, Ca(OH)2 hết → $n_{muối}$ = n $Ca(OH)_{2}$ =0,01 mol
m muối = 0,01*164=1,64 (g)
b. [Ca 2+]= $\frac{0,01}{0,5}$ = 0,02M
[NO3 -]= $\frac{0,02}{0,5}$ = 0,04M
[HNO3 dư]= $\frac{0,06}{0,5}$ = 0,12M