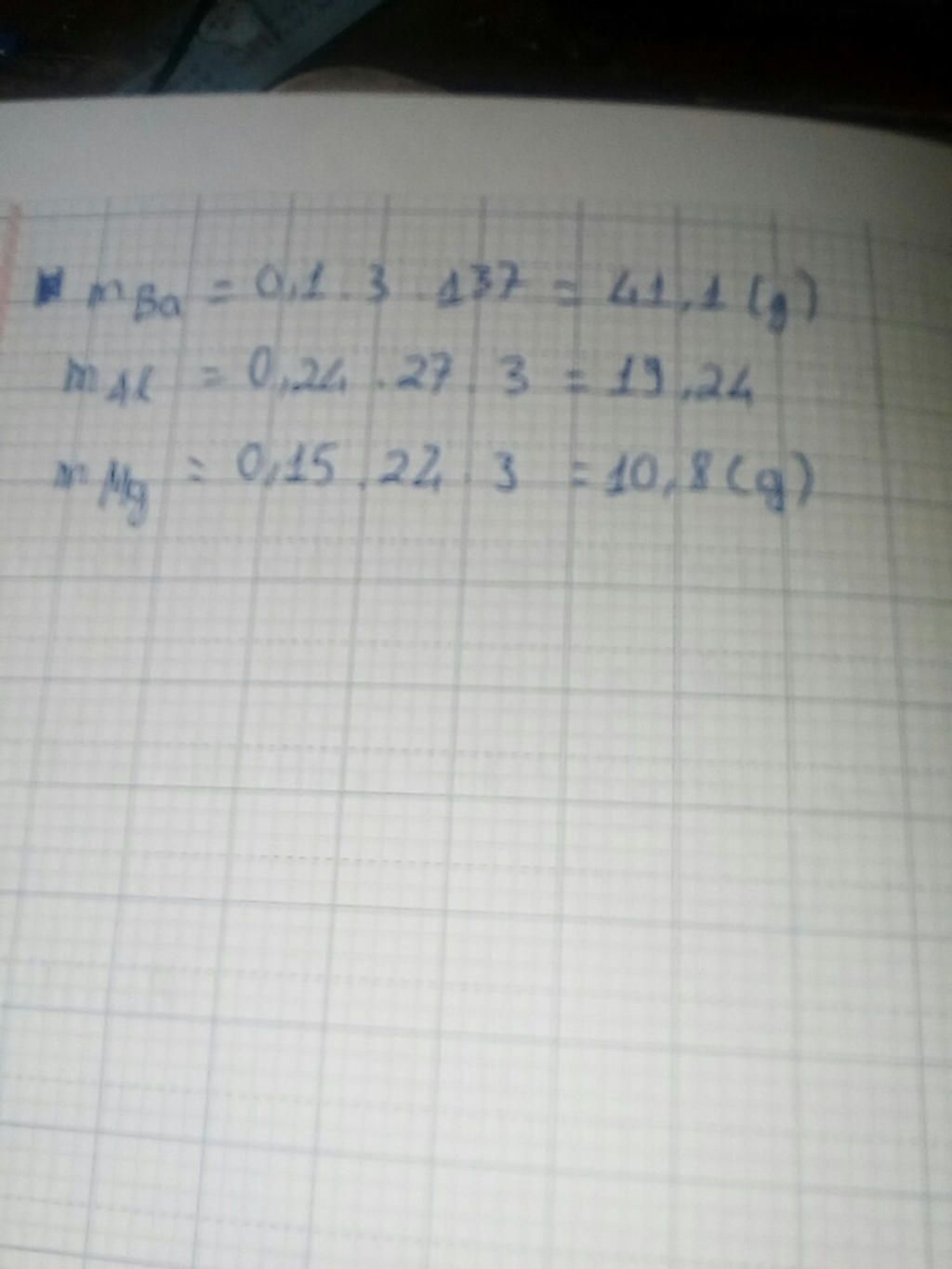Hỗn hợp A gồm Ba, Al, Mg được làm 3 phần bằng nhau: -Phần 1: Hòa tan vào nước dư thì sinh ra 8,96 lít khí H 2. -Phần 2: Hòa tan trong dd Ba(OH) 2 dư thì sinh ra 10,304 lít H 2. -Phần 3: Hòa tan trong dd H 2 SO 4 loãng, dư thu được 13,664 lít H 2. Các pư xảy ra hoàn toàn, các thể tích khí đo ở đktc. a) Viết các phương trình hóa học của phản ứng. b) Tính khối lượng mỗi kim loại trong A.
2 câu trả lời
Đáp án:
Giải thích các bước giải:
Gọi $n_{Ba} = a$ , $n_{Al} = b$ , $n_{Mg} = c$
$n_{H_2} (1) = 0,4 (mol)$
$n_{H_2} (2) = 0,46 (mol)$
$n_{H_2} (3) = 0,61 (mol)$
$Ba + H_2O → Ba(OH)_2 + H_2$
$Ba(OH)_2 + 2Al + 2H_2O → Ba(AlO_2)_2 + 3H_2$
Phần 1 thấy 0,4 < 0,46 => Ba hết , Al dư
$Ba + H_2SO_4 → BaSO_4 + H_2$
$2Al + 3H_2SO_4 → Al_2(SO_4)_3 + 3H_2$
$Mg + H_2SO_4 → MgSO_4 + H_2$
Ta có hpt
$\begin{cases} 4a=0,4\\a+1,5b=0,46\\a+1,5b+c=0,61 \end{cases}$ ⇔ $\begin{cases} a=0,1\\b=0,24\\c=0,15 \end{cases}$
$m_{Ba} = 0,1.3.137 = 41,1 (g)$
$m_{Al} = 0,24.27.3 = 19,24 (g)$
$m_{Mg} = 0,15.24.3 = 10,8(g)$
Câu hỏi trong lớp
Xem thêm