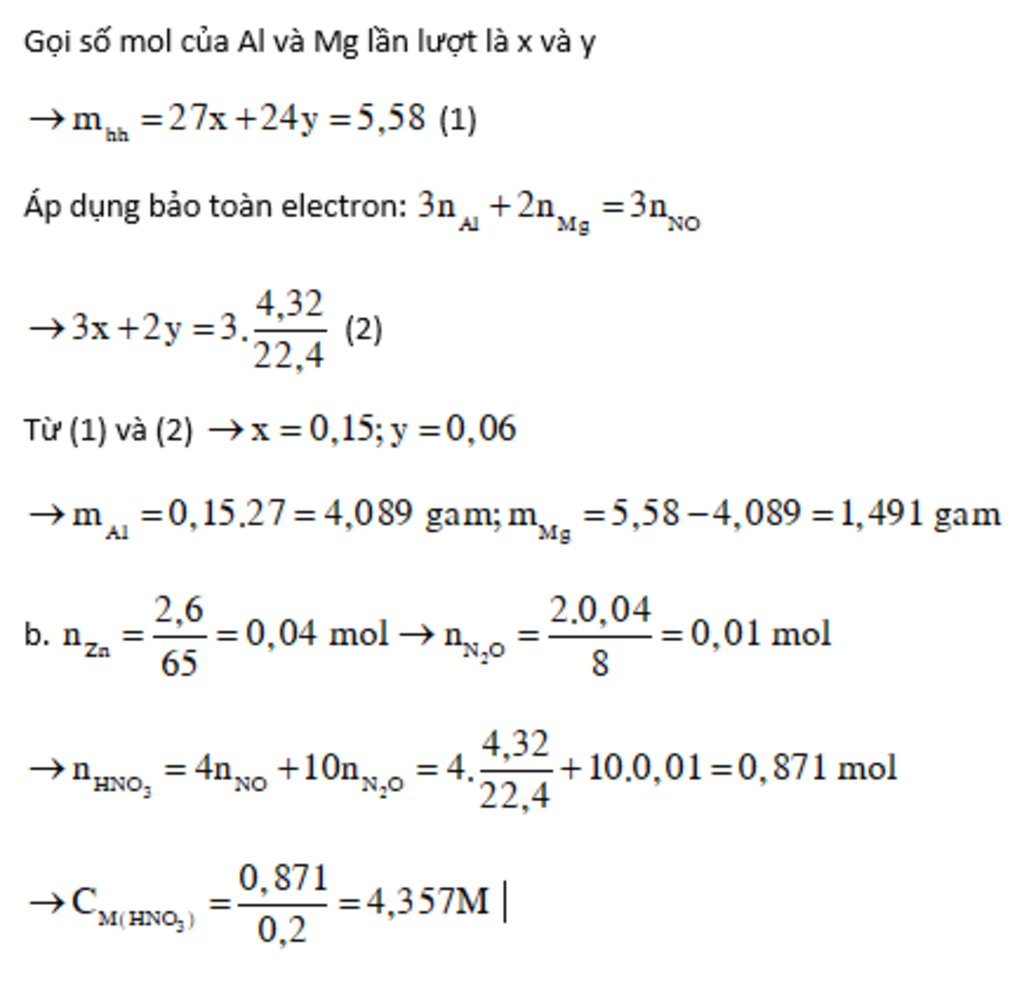Hòa tan hoàn toàn 5,58 g hỗn hợp hai kim loại Al và Mg trong 200ml dung dịch HNO3 loãng thu được 4,32 lít khí NO điều kiện tiêu chuẩn duy nhất và dung dịch A a )xác định khối lượng của Al và Mg trong hỗn hợp ban đầu b) xác định nồng độ mol của dung dịch HNO3 đã dùng ở trên biết rằng dung dịch A có thể hòa tan được 2,6 gam Zn và sinh ra khí N2O
2 câu trả lời
Đáp án:
a) $\eqalign{
& {m_{Al}} = 4,089(g) \cr
& {m_{Mg}} = 1,491(g) \cr} $
b) CM (HNO3) đã dùng = 4,357(l)
Giải thích các bước giải:
a) Gọi số mol Al, Mg là x, y
mhh = mAl + mMg
→ 27x + 24y = 5,58 (1)
nNO = 4,32 : 22,4 = $\frac{27}{140}$ mol
Al0 → Al+3 + 3e N+5 + 3e → N+2
x → x → 3x $\frac{81}{140}$ ← $\frac{27}{140}$
Mg0 → Mg2+ 2e
y → y → 2y
ADĐLBT e: ne nhường = ne nhận
→ 3x + 2y = $\frac{81}{140}$ (2)
Từ (1) và (2)
$\eqalign{
& \to \left\{ \matrix{
x = {{53} \over {350}} \hfill \cr
y = {{87} \over {1400}} \hfill \cr} \right. \cr
& {m_{Al}} = {{53} \over {350}}.27 = 4,089(g) \cr
& {m_{Mg}} = 5,58 - 4,089 = 1,491(g) \cr} $
b) nZn = 2,6 : 65 = 0,04 (mol)
Zn0 → Zn+2 +2e N+5 +4e → N+1
0,04 → 0,04 → 0,08 0,08→0,02
(BT e: ne nhường = ne nhận)
nN2O = $\frac{1}{2}$ nN+4 = 0,01 mol
Bảo toàn nguyên tố N:
nHNO3 đã dùng = 3nAl(NO3)3 + 2nMg(NO3)2 + nNO + nZn(NO3)2 + 2nN2O
= 3.$\frac{53}{350}$ + 2.$\frac{87}{1400}$ + $\frac{27}{140}$ + 2.0,04 + 2.0,01
= $\frac{61}{70}$ (mol)
CM (HNO3) đã dùng = $\frac{61}{70}$ : 0,2 = 4,357(l)