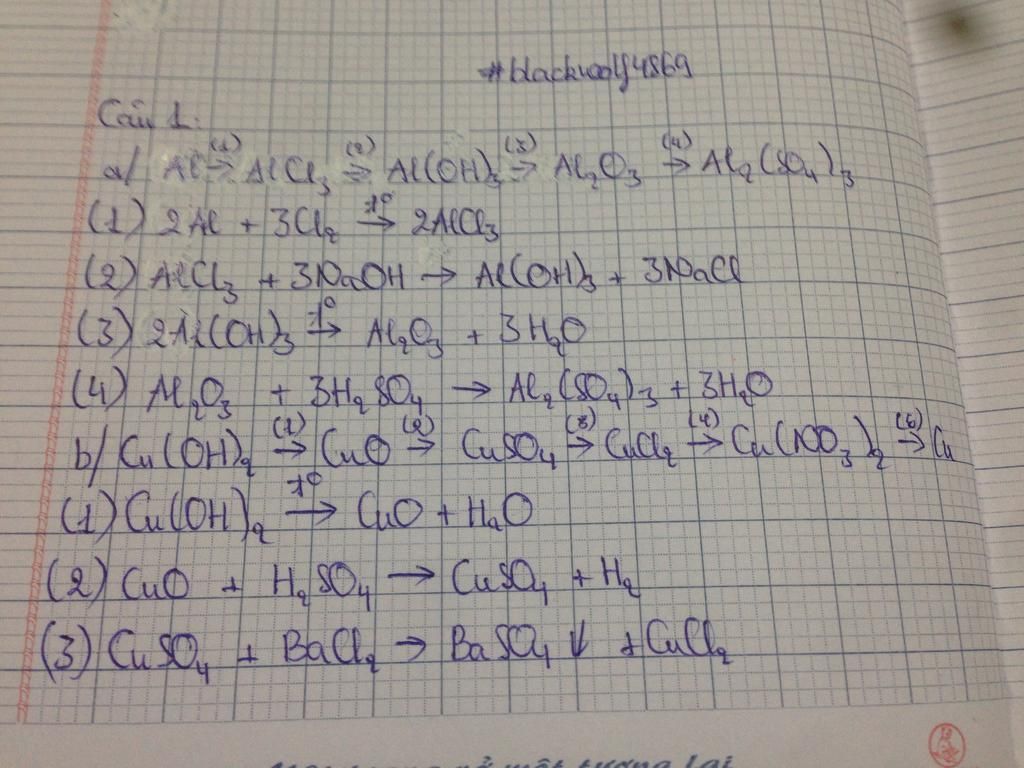giúp e bài này vs ạ... Câu 1:Viết PTHH thực hiện chuỗi biến hóa sau: a/Al →AlCl3→Al(OH)3→ Al2O3→Al2(SO4)3 b/Cu(OH)2 →CuO → CuSO4 →CuCl2 →Cu(NO3)2 → Cu Câu 2: Nhận biết dung dich: HCl, H2SO4, Ba(OH)2 Câu 3: Cho 10,5g hỗn hợp 2 kim loại Cu, Zn vào 500ml dung dịch H2SO4 loãng dư, thu được 2,24 lít khí (đktc). a/ Viết phương trình hoá học. b/Tính thành phần trăm khối lượng mỗi kim loại trong hỗn hợp? c/ Tính nồng độ mol dung dịch axit H2SO4 cần dùng?
2 câu trả lời
Câu 1:
$a,2Al+3Cl_2\xrightarrow{t^o}2AlCl_3\\ AlCl_3+3NaOH\to Al(OH)_3\downarrow+3NaCl\\ 2Al(OH)_3\xrightarrow{t^o}Al_2O_3+3H_2O\\ Al_2O_3+3H_2SO_4\to Al_2(SO_4)_3+3H_2O\\ b,Cu(OH)_2\xrightarrow{t^o}CuO+H_2O\\ CuO+H_2SO_4\to CuSO_4+H_2\\ CuSO_4+BaCl_2\to BaSO_4\downarrow+CuCl_2\\ CuCl_2+2AgNO_3\to 2AgCl\downarrow+Cu(NO_3)_2\\ Cu(NO_3)_2+Fe\to Cu\downarrow+Fe(NO_3)_2$
Câu 2:
Trích mẫu thử, cho quỳ tím vào các mẫu thử:
- Quỳ hóa đỏ: $HCl,H_2SO_4(1)$
- Quỳ hóa xanh: $Ba(OH)_2$
Cho dd $BaCl_2$ vào (1):
- Tạo kết tủa trắng: $H_2SO_4$
- Không hiện tượng: HCl
$BaCl_2+H_2SO_4\to BaSO_4\downarrow+2HCl$
Câu 3:
$a,PTHH:Zn+H_2SO_4\to ZnSO_4+H_2\\ n_{H_2}=\dfrac{2,24}{22,4}=0,1(mol)\\ b,n_{Zn}=n_{H_2}=0,1(mol)\\ \Rightarrow \%_{Zn}=\dfrac{0,1.65}{10,5}.100\%=61,905\%\\ \Rightarrow \%_{Cu}=100\%-61,905\%=38,095\%\\ c,n_{H_2SO_4}=n_{Zn}=0,1(mol)\\ \Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,1}{0,5}=0,2M$
Đáp án:
Bạn nhìn hình
Chữ hơi xấu nên mong bạn thông cảm ;-;
#blackwolf4869