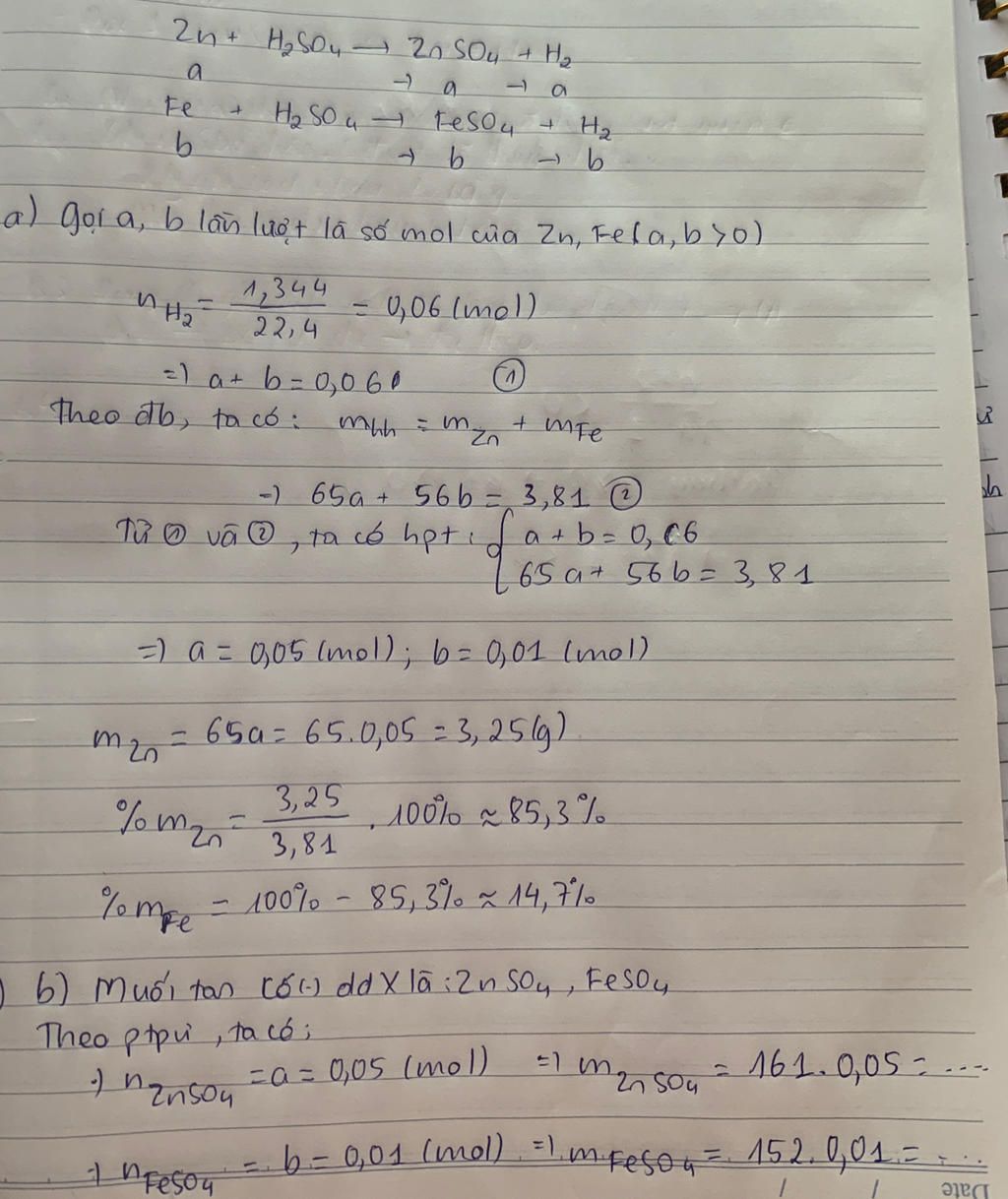Cho hỗn hợp gồm 3,81 gam hỗn hợp Kẽm, Sắt vào dung dịch H2SO4 loãng dư, thu được 1,344 lít khí H2 (đktc) và dung dịch X. a) Tính % khối lượng mỗi kim loại trong hỗn hợp? b) Xác định khối lượng các muối tan có trong dung dịch X?
2 câu trả lời
Đáp án:
Bạn tham khảo lời giải ở dưới nhé!!!
Giải thích các bước giải:
\(\begin{array}{l}
Zn + {H_2}S{O_4} \to Zn{\rm{S}}{O_4} + {H_2}\\
F{\rm{e}} + {H_2}S{O_4} \to FeS{O_4} + {H_2}\\
{n_{{H_2}}} = 0,06mol\\
\to {n_{Zn}} + {n_{Fe}} = {n_{{H_2}}} = 0,06mol
\end{array}\)
Mặt khác, ta có: \(65{n_{Zn}} + 56{n_{F{\rm{e}}}} = 3,81\)
Giải hệ phương trình ta có:
\(\begin{array}{l}
\left\{ \begin{array}{l}
{n_{Zn}} + {n_{Fe}} = 0,06\\
65{n_{Zn}} + 56{n_{F{\rm{e}}}} = 3,81
\end{array} \right.\\
\to {n_{Zn}} = 0,05mol \to {n_{Fe}} = 0,01mol\\
\to \% {m_{Zn}} = \dfrac{{0,05 \times 65}}{{3,81}} \times 100\% = 85,3\% \\
\to \% {m_{F{\rm{e}}}} = 100\% - 85,3\% = 14,7\% \\
\to {n_{Zn{\rm{S}}{O_4}}} = {n_{Zn}} = 0,05mol\\
\to {m_{Zn{\rm{S}}{O_4}}} = 8,05g\\
\to {n_{F{\rm{eS}}{O_4}}} = {n_{F{\rm{e}}}} = 0,01mol\\
\to {m_{FeS{O_4}}} = 1,52g
\end{array}\)