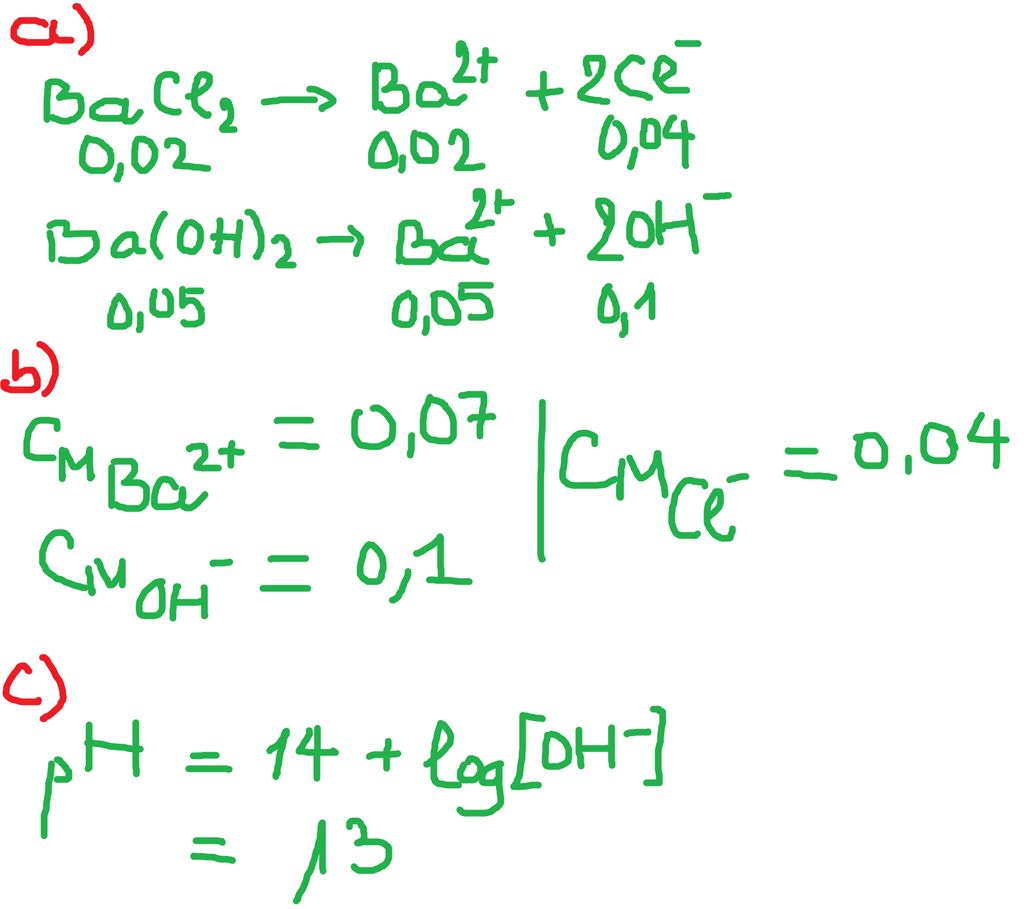Cho dung dịch X chức BaCl2 0,02M và Ba(OH)2 , 0,05M a. Viết PT điện li của các chất trong X( Bỏ qua sự điệu là của b. Tính nồng độ mạch các ion trong dung dịch pH của dung dịch X. c. Tính pH của dung dịch X
2 câu trả lời
Đáp án:
$BaCl_2 \to Ba^{2+} + 2Cl^{-}$
$Ba(OH)_2 \to Ba^{2+} + 2OH^{-}$
$[Ba^{2+}] =0,07M$
$[Cl^{-}] = 0,04M$
$[OH^{-}] = 0,1M$
$pH= 13$
Giải thích các bước giải:
Phương trình điện ly:
$BaCl_2 \to Ba^{2+} + 2Cl^{-}$
$Ba(OH)_2 \to Ba^{2+} + 2OH^{-}$
$[Ba^{2+}] = 0,02 + 0,05 = 0,07M$
$[Cl^{-}] = 2.0,02 = 0,04M$
$[OH^{-}] = 2. 0,05 = 0,1M$
$pOH = -log(0,1)=1$
$pH= 14-1=13$
Câu hỏi trong lớp
Xem thêm