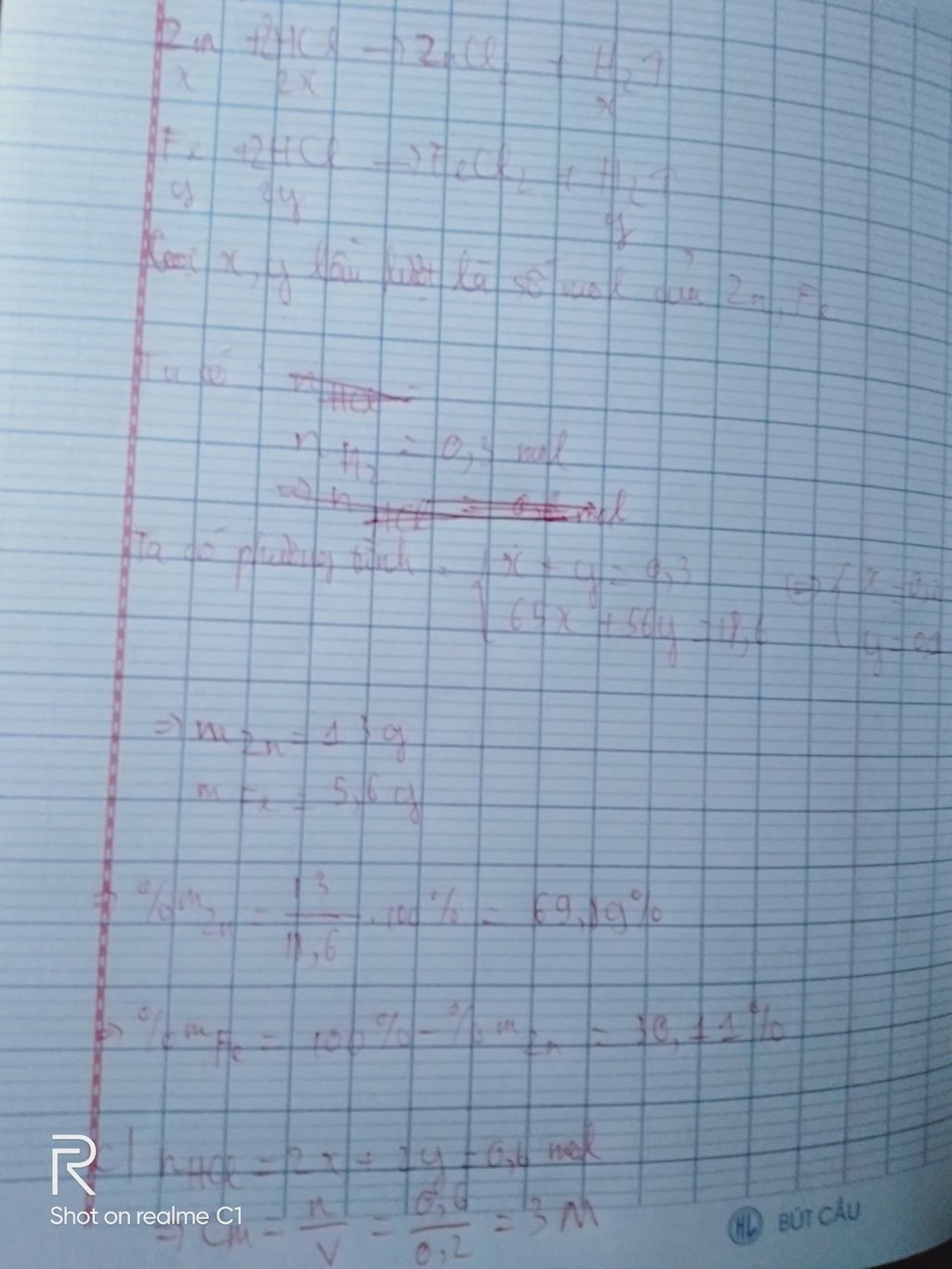
cho 18,6 (g) hỗn hợp A gồm Zn và Fe tác dụng vừa đủ vs 200ml đ HCL thấy có 6,72l khí thoát ra. a, viết PTHH xảy ra. b, tính % khối lượng Zn và Fe trong hỗn hợp ban đầu. c, tính CM của dd HCL đã phản ứng
2 câu trả lời
Đáp án:
Giải thích các bước giải: nH2= 6,72:22,4=0,3 mol
Zn + 2HCl → ZnCl2 + H2 (1)
mol x → 2x → x
Fe + 2HCl → FeCl2 + H2 (2)
mol y → 2y → y
18,6 (g) hỗn hợp A gồm Zn và Fe
⇒65x+56y=18,6
x+y=0,3
⇒x=0,2, y=0,1
⇒mFe=0,1.56=5,6(g)
⇒%mFe=5,6.100%:18,6=30,11%
⇒%mZn=100%-30,11%=69,89%
c, Theo PTHH (1) và (2): nHCl= 2x+2y=(0,2+0,1).2=0,6(mol)
⇒CMHCl = 0,6:0,2=3M
Câu hỏi trong lớp
Xem thêm