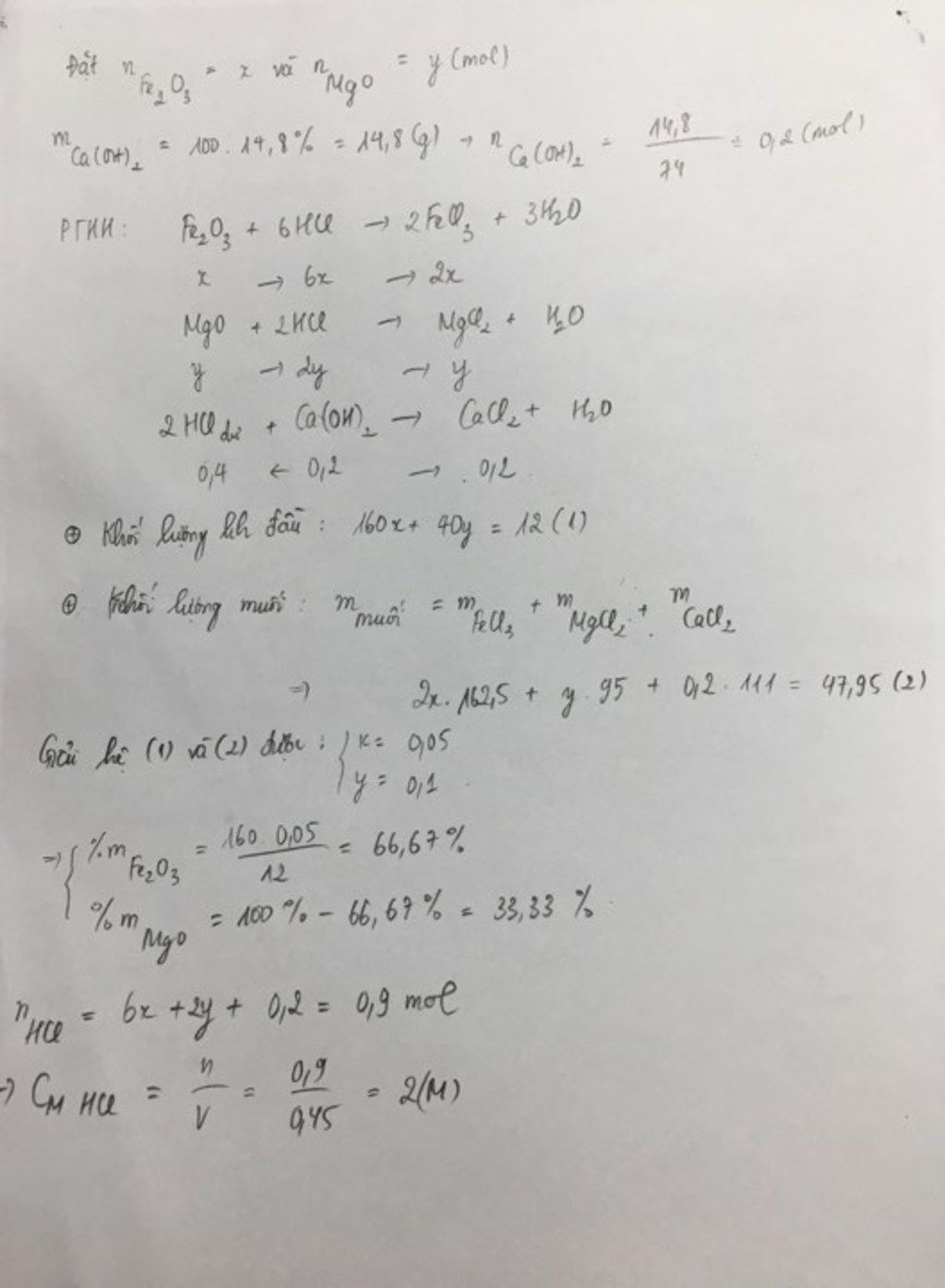Cho 12g hỗn hợp fe2O3,MgO hoà tan hết trong 450ml dd HCl sau phản ứng cần trung hoà axit dư bằng 100g dd Ca(OH)2 14,8%, sau đó cô cạn dd được 47,95g muối khan. Tính % khối lượng mỗi oxit trong hỗn hợp và nồng độ mol của HCl
2 câu trả lời
Đáp án:
Giải thích các bước giải: nCa(OH)2 = 0,2 mol
Gọi x,y lần lượt là số mol Fe2O3 và MgO
160x + 40y = 12
Dung dịch sau thu được có các ion : Fe3+ (2x), Mg2+ (y), Ca2+ (0,2), Cl-
nCl- = 6x + 2y + 0,4
-> 112x + 24y + 35,5.(6x+2y+0,4) + 0,2.40 = 47,95
-> x = 0,05, y = 0,1
-> % Fe2O3 = 66,67% -> %MgO = 33,33%
-> nHCl = 0,9 -> CM = 2
Câu hỏi trong lớp
Xem thêm