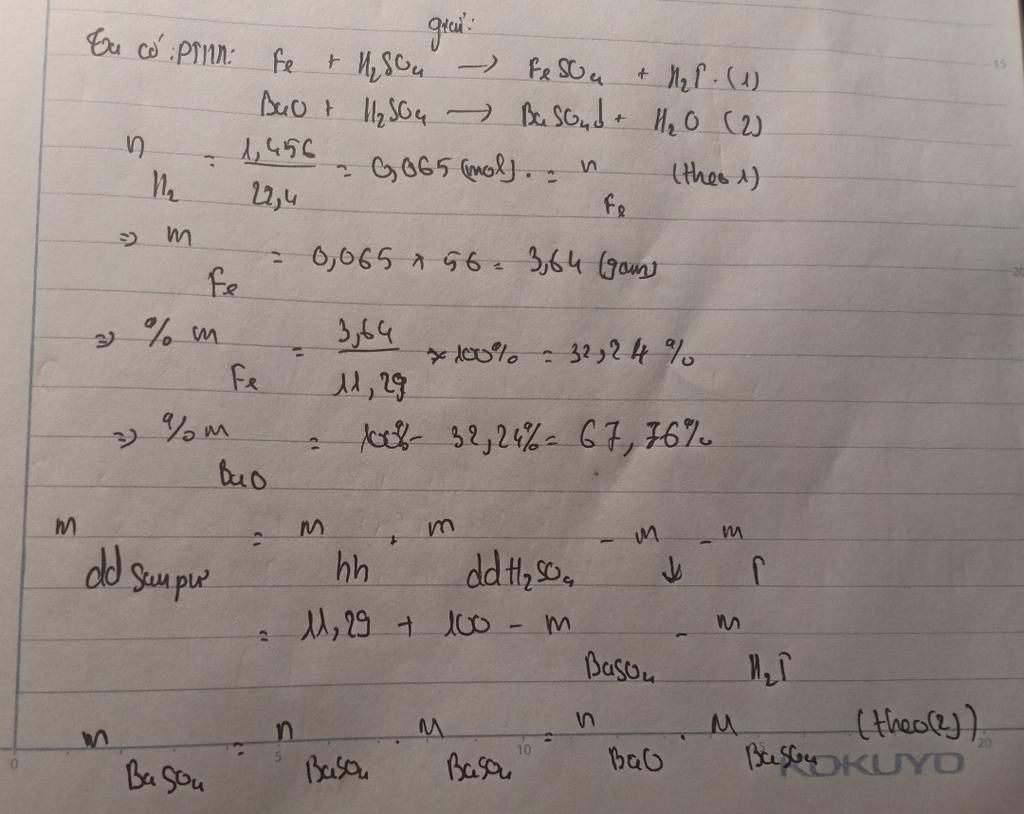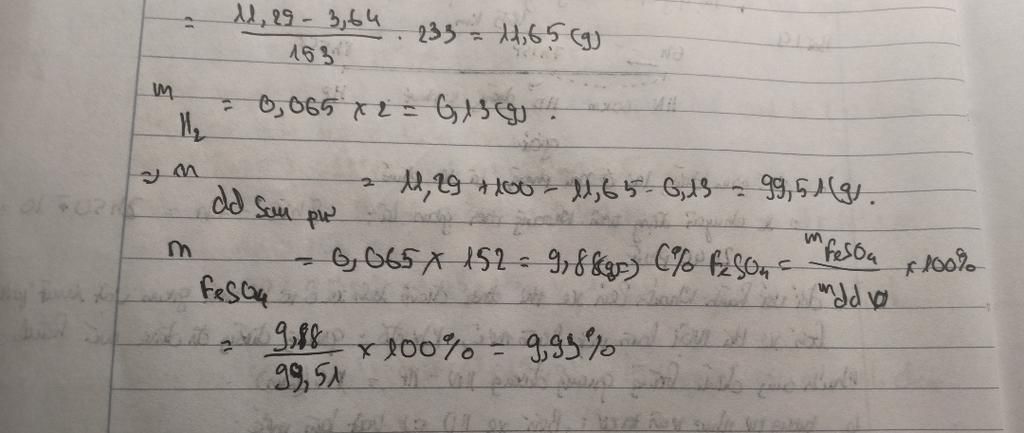cho 11,29g hỗn hợp Fe và BaO tác dụng hết với 100g dung dịch H2SO4 thu được 1,456 lít H2 (đktc) a, tính phần trăm theo khối lượng của Fe và BaO trong hỗn hợp b, tính C% của dung dịch sau phản ứng
2 câu trả lời
Em tham khảo nha :
\(\begin{array}{l}
a)\\
Fe + {H_2}S{O_4} \to FeS{O_4} + {H_2}\\
BaO + {H_2}S{O_4} \to BaS{O_4} + {H_2}O\\
{n_{{H_2}}} = \dfrac{{1,456}}{{22,4}} = 0,065mol\\
{n_{Fe}} = {n_{{H_2}}} = 0,065mol\\
{m_{Fe}} = 0,065 \times 56 = 3,64g\\
{m_{BaO}} = 11,29 - 3,64 = 7,65g\\
\% Fe = \dfrac{{3,64}}{{11,29}} \times 100\% = 32,2\% \\
\% BaO = 100 - 32,2 = 67,8\% \\
b)\\
{n_{BaO}} = \dfrac{{7,65}}{{153}} = 0,05mol\\
{n_{BaS{O_4}}} = {n_{BaO}} = 0,05mol\\
{m_{BaS{O_4}}} = 0,05 \times 233 = 11,65g\\
{n_{FeS{O_4}}} = {n_{Fe}} = 0,065mol\\
{m_{FeS{O_4}}} = 0,065 \times 152 = 9,88g\\
C{\% _{FeS{O_4}}} = \dfrac{{9,88}}{{11,29 + 100 - 11,65 - 0,065 \times 2}} \times 100\% = 12,84\%
\end{array}\)
Câu hỏi trong lớp
Xem thêm